Структура - катион
Cтраница 2
Энергия активации для этой перегруппировки найдена равной 137 кДж / моль, тогда как путь через структуру 7-норкарадиенильного катиона ( которая найдена нестабильной и является переходным состоянием) отвечает на 77 кДж / моль более высокому барьеру. Толиль-ные катионы проигрывают бензильному 48, 66 и 68 кДж / моль, соответственно, для орто -, мета - и пара-изомеров. Перегруппировка орто-толильного катиона в бензильный требует энергии активации в 105 кДж / моль, а барьер для перегруппировки орто -, жега-изомеров составляет 163 кДж / моль. [16]
Исследования, проведенные Харлоу [409], по изучению факторов, влияющих на устойчивость неводных растворов четвертичных аммониевых оснований и влияния структуры катиона на условия титрования кислот показали, что самыми устойчивыми титрантами являются гидроокиси тетраметил -, тетрабутил - и тетраэтиламмо-ния и наименее устойчивым - гидроокись триметилбензиламмо-ния. Устойчивость растворов увеличивается с увеличением содержания воды в титранте вследствие того, что относительно высокая кислотность воды понижает основность этих растворов и большая сольватирующая способность воды понижает степень ассоциации ионов титрантов. Однако увеличение содержания воды мешает определению очень слабых кислот и анализу смесей кислот различной силы. Разбавление спиртовых растворов нейтральными или основными растворителями с целью увеличения основности титрантов понижает их устойчивость. [17]
Для карбкатионов характерно большое многообразие реакций изомеризации ( перегруппировки), которые зачастую протекают с участием различных функциональных групп, входящих в структуру катиона. [18]
Однако для обоснованной аргументации такого положения требуется также учесть стабилизующее влияние окружения, так как это влияние может быть различным в зависимости от структуры катиона ( разд. [19]
В-третьих, процесс образования катионов при распаде диазо-ниевых солей протекает настолько быстро, что заместители около катионоидного центра не успевают принять планарное положение и структура катиона, в которой он далее реагирует, подобна структуре исходной диазониевой соли. По смыслу это аналогично тому, что, согласно постулату Хэммонда, строение активированного комплекса этой реакции подобно строению исходного соединения. Это определяет стереоспецифичность путей превращения получающихся катионов. [20]
При пропускании NH3 через водный раствор ЩАиСЦ ] в присутствии нитрата аммония образуется [ Аи ( ЫНз) 4 ] ( МОз) з с пло-скоквадратной структурой катиона. [21]
 |
Относительное изменение профилей потенциальной поверхности для ацилотропии в ряду эфиров 3 5 7-триметил-трополона при варьировании числа и расположения нитрогрупп в арильнон мигранте ( 25 С. [22] |
Это связано, во-первых, с оптимальной ориентацией электронного облака неподеленной пары электронов и атакующей группы, во-вторых, с тем, что в переходном состоянии один из фрагментов биполярного иона имеет структуру устойчивого катиона тропилия. [23]
Опыты по выравниванию метки, проведенные Робертсом и сотрудниками [78-81 ] для неустойчивого циклопропилметильного катиона, свидетельствуют, по нашему мнению, о быстрых перегруппировках. Структура катиона циклопропил - СН, которая следует из опытов по выравниванию метки [78-81], соответствует структуре равноделенной формы, с тем исключением, что в перекрывании участвует только одна половина р-орбиты. [24]
Косвенным доказательством структуры 2-норборнильного катиона ( 5) являются результаты исследования сольволитической циклизации 2 - ( циклопентен-3 - ил) этанола. [25]
Как много резонансных линий следует ожидать в спектре ЯКР на ядрах 1151п и 1271 для этого соединения при условии, что нет кристаллографической неэквивалентности аниона и катиона. О какой структуре катиона говорит такая небольшая величина. [26]
Вместе с отсутствием йлмяния природы катиона это означает, что в переходном состоянии - к: ут - OTRvET лоь илгкткые взаимодействия и что дгесольватшщя аниона является принципиальной стороной процесса активации. Заметная зависимость абсолютных констант скорости от структуры катиона указывает на то, что в переходном состоянии Y - и R не могут разделять слишком много молекул растворителя, и, как полагают, переходное состояние по структуре близко к единичной сольватно-разделенной ионной паре ( гл. [27]
Четвертичные аммониевые соли с короткой алкильной цепью обладают в воде поверхностно-активными свойствами и образуют мицеллы. Критическая концентрация мицеллообразования зависит кроме температуры от структуры катиона, природы аниона и присутствия, электролита в растворе. [28]
Красители с алкильными заместителями в положениях 3 3 и 9 отличаются от красителей первой группы тем, что пространственные затруднения, связанные с наличием объемистых заместителей в этих положениях, препятствуют плоскому расположению гетероциклических ядер. Пространственные затруднения иллюстрируются рис. 8 и 9 для растянутой структуры катиона. Аналогичные схемы для других конфигураций показывают, что в присутствии алкильных групп плоские структуры всегда приводят к перекрыванию сфер действия вандерваальсовых сил. [29]
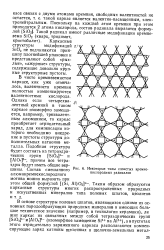 |
Некоторые типы слоистых кремие-кислородиых радикалов. [30] |
Страницы: 1 2 3