Структура - кислота
Cтраница 3
Жирные и другие органические кислоты, присутствующие в осадочных отложениях, представляют интерес как исходный материал, поскольку достаточно, чтобы из структуры кислоты была удалена двуокись углерода, и в остатке получается соответствующий углеводород. Действительное превращение органических кислот с образованием углеводородов имеет, как это описано ниже, более сложный характер, но эти кислоты являются несомненным источником углеводородов. [31]
Обычно точные предсказания об относительной кислотности в пиридине могут быть сделаны при наличии данных о константах диссоциации в воде и если принята во внимание структура кислот. [32]
Получены полимеркаптостирол56Э6 и полимеркаптометилсти-рол 5697, проведено взаимодействие полистирола с фталоилдихло-ридом 5698, приводящее к образованию полимера, содержащего в зависимости от температуры реакции структуры о-бензоилбен-зойной кислоты или антрахинона. [33]
Оценка кинетических данных, полученных при определении скоростей расщепления эфиров гидроксиламином и омыления при рН 9 8, показала, что на реакционную способность эфирной связи сильно влияет структура кислоты, атом кислорода, находящийся в кольце углевода, и соседняя гидроксильная группа. Индукционный и стерический эффекты, а также образование водородных связей, вполне возможно, играют важную роль в образовании нового состояния связи, которую несколько произвольно называют макроэргической связью. Заметное влияние также может оказывать соседняя фосфатная группа [31], по-видимому, вследствие нуклеофильной атаки анионом фосфата карбонильной группы эфира с образованием переходного аминоацил-фосфатного ангидрида. [34]
Первые же исследования ионообменных свойств сурьмяной кристаллической кислоты ( СКК) привели к естественному отказу от эмпирической формулы Sb2O5 - nH2O и заставили искать связь способности к обмену ионов со структурой кислоты. [35]
И то, что стабилизация иона будет, таким образом, больше, чем стабилизация самой кислоты, и то, что в результате положительного знака на гидроксильном кислороде во второй структуре кислоты будет происходить отталкивание протона, говорит о карбоновых кислотах, как о силышх кислотах ( ср. [36]
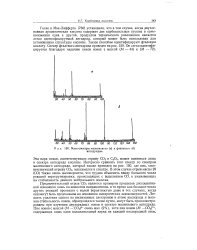 |
Масс-спектры малеинового ( а и фталевого ( б ангидридов. [37] |
Голке и Мак-Лафферти [760] установили, что в том случае, когда двухосновная ароматическая кислота содержит две карбоксильные группы в орто-положении одна к другой, продуктом термического разложения является легко идентифицируемый ангидрид, который может быть использован для установления структуры кислоты. Таким способом идентифицируют фталевую кислоту. [38]
Очевидно, что этот метод является более трудоемким, чем реакция Фриделя - Крафтса; однако его часто применяют в тех случаях, когда ацетилнрование и реакция с янтарным ангидридом направляются в различные положения ядра, а также с целью доказательства структуры кислот, получаемых при реакции с янтарным ангидридом. Если всходить из арилэтилкетона, то можно получить р-метил - - арощшропйОиовые кислоты, менее доступные при прямой реакции с янтарным ангидридом. Применение эфира метил малоновой кислоты позволяет синтезировать сс-метил - - ароилпропионовые кислоты. [39]
Структуры гемо -, крипто -, опсо - и ФИЛЛШ1ИРРОЛ 01В были выяснены путем превращения их в производные гшррола установленного строения и целого ряда взаимных превращений. Структура пирролкарбоно-вых кислот была установлена декарбоксилированием их в соответствующие пирролы и окислением в гематиновую кислоту. [40]
В водном растворе разряд карбоксилатов возможен лишь на анодах из гладкой платины и иридия или из углерода. Если структура кислоты такова, что может образоваться продукт сочетания, то для получения его с оптимальным выходом слстуе. Реакция Кольбе может быть проведена на стеклоуглероде и спеченном угле [26, 28] Для пиролитического углерода распределение продуктов зависит от тою, проводится ли реакция на гранях или плоскостях электрода [28]; это подтверждает, что различия связаны с адсорбционными свойствами. [41]
Правильность структуры кислоты I позднее была подтверждена синтезом и, кроме того, при помощи ИК-спектров было показано, что синтетическая кислота I идентична Сгт-фтиеновой кислоте Кэзона ( С. [42]
Мичович [670] провел повторные исследования и показал, что кислоты Энгель-гарда и Пфитцингера идентичны. О структуре кислоты можно заключить по следующим реакциям, в которых участвует метальная группа, находящаяся в положении 2 хинолинового ядра. [43]
Рассмотрим вопросы о строении комплексов Zr4 n Ш4 с оксикислотами. Введение ОН-группы в структуру кислоты приводит к усилению кислотных свойств органического реагента, что в известной степени способствует реакциям комплексообразования. Однако, на наш взгляд, более существенным фактором является возможность замыкания пятичленного цикла при комплексообразовании с а-оксикислотами. [44]
Рассмотрим вопросы о строении комплексов Zr4 и Ш4 с окси кислотами. Введение ОН-группы в структуру кислоты приводит к усилению кислотных свойств органического реагента, что в известной степени способствует реакциям комплексообразования. Однако, на наш взгляд, более существенным фактором является возможность замыкания пятичленного цикла при комплексообразовании с сс-оксикислотами. [45]
Страницы: 1 2 3