Структура - активированный комплекс
Cтраница 2
В связи с рассмотренными явлениями представляет интерес обсуждение структуры активированного комплекса при электролитическом выделении водорода. [16]
Хэммонда дает правильные предсказания о направлении изменений в структуре активированного комплекса. По-видимому, только две серии работ находятся в противоречии с развиваемой концепцией. На возможных причинах несоблюдения постулата Хэммонда мы остановимся несколько позднее. [17]
Прежде всего следует указать, в чем заключается утрирование структуры активированного комплекса. В качестве примера рассмотрим структуру активированного комплекса бензола при электрофильном замещении ( см. рис. 16.25): предполагается, что гибридизация атома углерода, на котором осуществляется замещение, близка к состоянию sp3; это означает, что сопряжение ослаблено, однако не разрушено полностью. [18]
Анализ последней характеристики помогает составить представление о составе и структуре активированного комплекса лимитирующей стадии и приблизиться таким путем к выяснению механизма суммарного процесса. [19]
В то же время q ( 1 растет и даже сама структура активированного комплекса может меняться. [20]
И хотя, как правило, экспериментально невозможно установить, какова структура активированного комплекса, обычно удается создать о нем довольно, реальное представление. [21]
И хотя, как правило, экспериментально невозможно установить, какова структура активированного комплекса, обычно удается создать о нем довольно реальное представление. [22]
 |
Модель молекулы этилена. [23] |
На рис. 35 и 36 изображены ми-лекулы этилена и принятая для расчета структура активированного комплекса. [24]
Рассмотренный пример показывает, что даже в случае двух атомов необходимо делать предположение о структуре активированного комплекса; и эта проблема сильно усложняется, когда число атомов растет. Однако имеется другая простая, но важная иллюстрация его применения. Рассмотрим влияние дейтерирова-ния на скорость разрыва связи С - И. Общая кривая реакции не опускается, поскольку соответствующие колебания активированного комплекса очень свободны и, следовательно, имеют небольшую нулевую энергию как Для протонной, так и для дейтериевой форм. [25]
Рассмотренный пример показывает, что даже в случае двух атомов необходимо делать предположение о структуре активированного комплекса; и эта проблема сильно усложняется, когда число атомов растет. Однако имеется другая простая, по важная иллюстрация его применения. Рассмотрим влияние дейтерирова-чия на скорость разрыва связи С - И. Общая кривая реакции не опускается, поскольку соответствующие колебания активированного комплекса очень свободны и, следовательно, имеют небольшую нулевую энергию как Для протонной, так и для дейтериевой форм. [26]
Константа равновесия ее выразится произведением К KZK3 - Объединение медленных стадий недопустимо, так как структура активированных комплексов в них весьма существенна для понимания механизма всего процесса. Ясно, что изменение энергии Гиббса AG в быстрых стадиях близко к нулю, в силу их равновесности, а все изменения AG для данного процесса сосредоточиваются в медленных стадиях. [27]
 |
Принцип Хаммонда. [28] |
В заключение следует сказать, что из значений активационных параметров, в особенности из Д5Ф, можно делать выводы о структуре активированных комплексов. Получение о них каких-либо определенных представлений позволяет установить механизм элементарной реакции. [29]
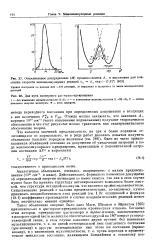 |
Относительное распределение ( М предэксионентов А, в выражении для константы скорости мономолекулярных реакций k Аа ехр ( - EIRT.| Два пути изомерного ццс-тракопревращения. [30] |
Страницы: 1 2 3 4