Структура - активированный комплекс
Cтраница 4
Как видно из рассмотрения схемы ( 3), структура метанола образу - - ется в результате переноса гидрид-иона к карбониевому центру, являющемуся акцептором электронной пары. При этом мигрирующий гидрид-ион не переходит в раствор, а перемещается внутри структуры активированного комплекса. Однако в работе Ш не были приведены экспериментальные доказательства справедливости данного механизма. [46]
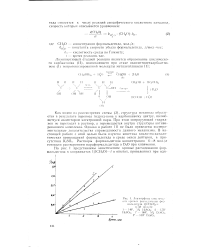 |
Лнаморфсиы киииичоо-кпх кршшх расхол. О Н. шия формальдегида ( [ С1ЬО ] о. [47] |
Как видно из рассмотрения схемы ( 3), структура метанола образуется в результате переноса гидрид-иона к карбониевому центру, являющемуся акцептором электронной пары. При этом мигрирующий гидрид-ион не переходит в раствор, а перемещается внутри структуры активированного комплекса. Однако в работе 1.1 ] не были приведены экспериментальные доказательства справедливости данного механизма. Растворы формальдегида концентрации б - 8 мол. [48]
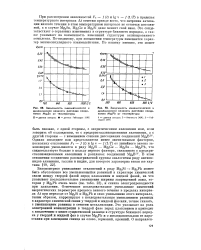 |
Зависимость кинематической и динамической вязкости расплава соединения MgjSn от температуры.| Зависимость кинематической и динамической вязкости расплава соединения iMgjPb от температуры. [49] |
При рассмотрении зависимостей РЪ - / ( t) и lg v - / ( 1 / 71) в пределах температурного интервала At отметим прежде всего, что энтропия активации вязкого течения в этом температурном интервале не остается постоянной, а в случае Mg2Sn, Mg2Ge и Mg2Si даже меняет свой знак. Это свидетельствует о серьезных изменениях в структуре ближнего порядка, а также указывает на возможность изменений структуры активированного комплекса. По-видимому, при повышении температуры изменяется характер межмолекулярного взаимодействия. [50]
 |
Относительное распределение ( Л / нред-экспонентов А в выражении для константы скорости мономолекулярных реакций k03. [51] |
Аналогичное объяснение, очевидно, не применимо к малым предэкспо-нентам порядка 1011 и ниже. Действительно, формально возможное допущение об отрицательной энтропии активации не имеет смысла, так как в этом случае нужно было бы принять структуру активированного комплекса более жесткой, чем структура исходной молекулы, что крайне маловероятно. [52]
Так, в 1969 г. Ф. Б. Моин 1275 ] рассмотрел экспериментальные данные по кинетике элементарных газофазных реакций молекул, опираясь на представление о структуре активированного комплекса как молекулы с активированными ( более слабыми, чем химические) связями. Исходя из постулата, что кинетика процесса определяется структурой переходного комплекса, автор считает, что именно поэтому кинетику реакций определяют активированные связи, а химические связи, не образующие этого комплекса, довольно слабо влияют на протекание процесса. Сильно понижающее влияние на энергию активации оказывает наличие сопряженных и кумулированных л-связей в активированном комплексе. [53]
Изотопный эффект дейтерия особенно важен для исследования химических реакций с участием органических соединений, так как из измерений изотопного эффекта можно установить, является ли разрыв С - Н связи скоростьопределяющей стадией. В настоящее время не имеется достаточно точного метода теоретического расчета изотопного эффекта главным образом потому, что отсутствует достаточное количество данных о структуре активированного комплекса. Ниже приводится грубая оценка изотопного эффекта исходя из уравнения Аррениу-са ( разд. [54]
 |
Два пути изомерного цыс-тракопревраще-ния. [55] |
Аналогичное объяснение не применимо к реакциям с малыми предэкспоненциальными множителями ( порядка 10й и ниже), поскольку предположение об AS 0 означает, что структура активированного комплекса более жесткая, чем исходной молекулы, а это крайне маловероятно. Столь низкие значения А объясняются неадиабатическим протеканием реакции. [56]
Влияние растворителя и структуры реагентов на скорость реакции проявляется через влияние на свободную энергию исходных реагентов и активированного комплекса. Для учета этого влияния необходимо знать в деталях структуру активированного комплекса и природу взаимодействия реагирующих частиц с растворителем, который, строго говоря, входит в структуру активированного комплекса. Однако, за редким исключением, эта информация у исследователя отсутствует. [57]
Этот принцип гласит: если переходное состояние и ближайшее соседнее состояние имеют почти равные энтропии, то переход от одного к другому требует крайне малых изменений молекулярной структуры. На рис. 1.5.8 ( а) приведены диаграммы двух сильно экзотермич-ных реакций. Структуры активированных комплексов аналогичны структуре реагентов. Различия в ДРЯ почти не влияют на ДЯФ. [58]
Страницы: 1 2 3 4