Структура - хлористый натрий
Cтраница 3
В газообразном состоянии влияние структуры иона аммония становится более резко выраженным. В кристаллическом состоянии вращающийся ион аммония напоминает ион рубидия: он имеет такой же самый кажущийся размер, и из табл. 20 и 28 видно, что NH4I, имеющий структуру хлористого натрия, имеет почти такую же энергию решетки, как Rbl. Энергии решеток других аммонийных солей, не имеющих структуры хлористого натрия, за исключением фтористого аммония, также не сильно отличаются от энергий солей рубидия. [31]
Положительные ионы находятся в дырках между отрицательными ионами. Исследование множества ионных соединений позволяет составить таблицы ионных радиусов, подобные приведенной на рис. 4.9. Аддитивность этих величин иллюстрируется в табл. 14.6 сопоставлением с наблюдаемыми межъядерными расстояниями в кристаллических соединениях, имеющих структуру хлористого натрия. [32]
Точка плавления фторидов щелочно-земельных металлов находится в пределах от 700 до 1000 С. В большинстве своем они являются ионными соединениями из-за большого различия в величине электроотрицательности атомов, входящих в их состав. Кристаллы бесцветны, обладают структурой хлористого натрия. Согласно данным исследования поглощения этих кристаллов в ультрафиолетовом свете, ширина запретной зоны составляет 10 эв. [33]
Довольно часто ограниченный интервал смешанных кристаллов образуют и вещества, не изоморфные друг с другом. С другой стороны, изоморфные соединения отнюдь не всегда дают смешанные кристаллы. KBr, KI и PdS все имеют структуру хлористого натрия и изоморфны. КВг дают полный ряд смешанных кристаллов, но КС1 и K. I образуют смешанные кристаллы только в ограниченном интервале составов, безусловно, вследствие отличия в размерах между Г и СГ. Далее, КС1 и PdS вообще не дают смешанных кристаллов; по-видимому, типы связей в этих двух соединениях сильно отличаются друг от друга. [34]
В газообразном состоянии влияние структуры иона аммония становится более резко выраженным. В кристаллическом состоянии вращающийся ион аммония напоминает ион рубидия: он имеет такой же самый кажущийся размер, и из табл. 20 и 28 видно, что NH4I, имеющий структуру хлористого натрия, имеет почти такую же энергию решетки, как Rbl. Энергии решеток других аммонийных солей, не имеющих структуры хлористого натрия, за исключением фтористого аммония, также не сильно отличаются от энергий солей рубидия. [35]
 |
Влияние отношения радиусов. [36] |
Действительно, при высоких давлениях галогениды рубидия переходят в эту структуру. С другой стороны, отношение радиусов для хлорида, бромида и иодида лития выходит за нижний предел для координации 6: 1, так что у этих соединений следовало бы ожидать осуществления структуры сульфида цинка. На самом деле все эти соли лития имеют структуру хлористого натрия, и ионы лития болтаются в октаэдри-ческих дырках, образованных плотноупакованной решеткой анионов ( см. стр. [37]
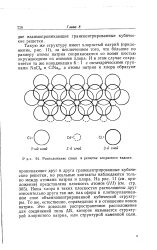
Можно считать, что в некоторых простых структурах, которые осуществляются в кристаллах простых ионных соединений, большие ионы ( обычно анионы) образуют плотневшую упаковку. Ланде указал в 1920 г., что это справедливо для структуры хлористого натрия. В галогенидах лития имеются плотно упакованные решетки анионов, которые в основном определяют значения констант решеток. Это заключение относительно структуры хлористого натрия должно быть приписано Барлоу. В 1898 г. он указал, что в этой структуре, состоящей из шаров с отношением радиусов 0 414 ( изображенной на рис. 1, взятым из работы Барлоу), большие шары образуют кубическую плотнейшую упаковку. [38]
Два других низших фторида молибдена описаны лишь очень кратко. Ше-стифтористый молибден реагирует с. Последние представляют собой белые вещества, водные растворы которых окрашены в синий цвет; NaMoF6 имеет структуру хлористого натрия, KMoF3 изоморфен KTaF6, а рубидиевая соль обладает ромбоэдрической структурой BaSiFe. Если калиевую соль сплавлять с большим избытком бифторида калия и полученную массу выщелачивать ацетоном, содержащим небольшое количество воды, остается бледно-зеленый комплекс KaMoOFs. Гексафто - po - ( V) молибдаты подчиняются закону Кюри-Вейсса и обладают очень высокими значениями 0; их магнитные моменты в соответствии с наличием одного неспаренного электрона134 при комнатной температуре составляют 1 5 - 1 75 магнетона Бора. [39]
Радиусы ионов щелочного металла и галоида были определены из расстояний в кристаллах, состоящих из одновалентных ионов и имеющих структуру хлористого натрия, а радиусы других ионов в табл. 16 в действительности представляют протяженность в пространстве электронного облака вокруг иона, определенного сравнением с ионами галоида и щелочного металла. Отсюда следует, что расстояния в кристалле должны передаваться такими радиусами только в том случае, если кристалл состоит из одновалентных ионов и имеет структуру хлористого натрия. Но, понятно, поливалентные ионы не могут образовать кристалл, состоящий из одновалентных ионов, а также кристаллы могут и не иметь структуры хлористого натрия. [40]
Обе эти структуры изображены на рис. 15.13, где указано также, какие галогениды обладают той или иной структурой при обычных лабораторных условиях. Повышение или понижение температуры или давления может привести к модификации одной кристаллической формы в другую структуру. Так, RbCl, RbBr и Rbl при давлении выше 5000 кг / см2 приобретают структуру хлористого цезия, a CsCl при температуре выше 460 С переходит в модификацию со структурой хлористого натрия. [42]
Другие кристаллы галогенидов щелочных металлов еще более ионные; в кристаллическом хлористом натрии, например, связи имеют около 5 % ковалентного характера. Интересно рассмотреть с этой точки зрения галогениды серебра. Это приводит к 11 % ионного характера для молекулы AgJ, 23 % - для AgBr, 30 % - для AgCl и 70 % - для AgF. В кристаллах фторида, хлорида и бромида, которые имеют структуру хлористого натрия, связи имеют, соответственно, 5, 12 и 13 % ковалентного характера. Эти величины получены в предположении, что в кристалле одна связь резонирует между шестью положениями; аналогичный подход к иодиду со структурой вурцита приводит к 23 % ковалентного характера для каждой из четырех связей, образованных атомом серебра. Однако, возможно, что эти степени ковалентного характера для связей в кристаллах должны быть удвоены по следующим причинам. [43]
 |
Расположение слоев в решетке хлористого кадмия. [44] |
На рис. 11 ( см. приложение) представлена плоскость атомов ( 111) ( см. стр. Ионы хлора в таких плоскостях расположены друг относительно друга так же, как сферы в плотноупакован-ном слое объемноцентрированной кубической структуры. То же, естественно, справедливо и в отношении ионов натрия. Это довольно распространенное расположение для соединений типа АВ, которое называется структурой хлористого натрия, или структурой каменной соли. [45]
Страницы: 1 2 3 4
