Структура - хлористый натрий
Cтраница 4
А ( см. табл. 18) и, следовательно, с меньшей энергией решетки, если считать, что межатомные расстояния меняются незначительно. В случае фтористого аммония кристалл имеет структуру вюрцита, повидимому, потому, что ион фтора настолько мал, что он может подойти достаточно-близко к иону аммония и сделать заметной энергию, появляющуюся вследствие нарушения симметрии. С другой стороны, хлористый и бромистый аммоний имеют структуру хлористого цезия, а йодистый аммоний - структуру хлористого натрия и структуру хлористого цезия при температурах ниже - 15 С, причем вероятно, что ион аммония имеет свободное вращение при комнатной температуре. Во всяком случае, недостаток сферической симметрии выражается нерезко. [46]
Радиусы ионов щелочного металла и галоида были определены из расстояний в кристаллах, состоящих из одновалентных ионов и имеющих структуру хлористого натрия, а радиусы других ионов в табл. 16 в действительности представляют протяженность в пространстве электронного облака вокруг иона, определенного сравнением с ионами галоида и щелочного металла. Отсюда следует, что расстояния в кристалле должны передаваться такими радиусами только в том случае, если кристалл состоит из одновалентных ионов и имеет структуру хлористого натрия. Но, понятно, поливалентные ионы не могут образовать кристалл, состоящий из одновалентных ионов, а также кристаллы могут и не иметь структуры хлористого натрия. [47]
Ряд галогенидов серебра часто приводят в качестве примера группы соединений, ярко иллюстрирующей переход от ионной к ковалентной связи. При рассмотрении приведенных в таблице данных видно, что расхождение между наблюденными межядер-ными расстояниями и вычисленными межионными расстояниями постепенно возрастает при переходе от AgF к Agl. Подобным же образом и различия между экспериментально найденной и теоретически вычисленной энергией решетки также последовательно увеличиваются. Разумеется, этот тип решетки можно ожидать и при ионной связи, если отношение радиусов катиона и аниона достаточно мало; однако в случае Agl оно недостаточно мало и иодиды щелочных металлов, имеющие катионы меньших размеров, чем Ag, обладают структурой хлористого натрия. В дополнение к рассмотренным до сих пор свойствам предполагается, что уменьшающаяся от фтора к иоду растворимость серебряных солей непосредственно связана с увеличением ковалентного характера связи в указанной последовательности. Это обсуждается в § 19.7. Ход изменения всех свойств этих веществ, таким образом, согласуется с ходом изменения характера связи. [48]
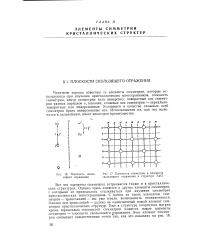 |
Плоскость скользящего отражения.| Плоскости симметрии и плоскости скользящего отражения в структуре NaCl. [49] |
Все эти элементы симметрии встречаются также и в кристаллических структурах. Однако здесь имеются и другие элементы симметрии, с которыми не приходилось сталкиваться при изучении симметрии кристаллических многогранников. Однако оси трансляций - далеко не единственный новый элемент симметрии кристаллических структур. Уже в структуре хлористого натрия кроме зеркальных плоскостей симметрии имеются новые элементы симметрии - плоскости скользящего ртражения. [50]
Можно считать, что в некоторых простых структурах, которые осуществляются в кристаллах простых ионных соединений, большие ионы ( обычно анионы) образуют плотневшую упаковку. Ланде указал в 1920 г., что это справедливо для структуры хлористого натрия. В галогенидах лития имеются плотно упакованные решетки анионов, которые в основном определяют значения констант решеток. Это заключение относительно структуры хлористого натрия должно быть приписано Барлоу. В 1898 г. он указал, что в этой структуре, состоящей из шаров с отношением радиусов 0 414 ( изображенной на рис. 1, взятым из работы Барлоу), большие шары образуют кубическую плотнейшую упаковку. [51]
Сплавы, содержащие элементы первых подгрупп В, имеют типичные металлические свойства. Твердые растворы образуются в более широком интервале только элементами одной подгруппы, при условии выполнения критерия относительных размеров атомов. Например, кадмий и ртуть образуют твердые растворы в очень большом интервале состава, а кадмий и цинк - в малом интервале; следует напомнить, что радиусы цинка, кадмия и ртути равны соответственно 1 37, 1 52 и 1 55 А. С другой стороны, кадмий и олово практически не смешиваются. Если оэа металла принадлежат к последним подгруппам В, то в ряде случаев образуется соединение, имеющее структуру хлористого натрия, например SnSb, SnTe, PbSe и РЬТе. Примерами соединений с этими структурами являются сульфиды, селениды и теллуриды цинка, кадмия и ртути, а также GaAs, GaSb и InSb. Соединения типа BeS и А1Р также кристаллизуются в структуре цинковой обманки, которая встречается не только в элементах подгруппы В. [52]
Функция распределения электронов в ионе не имеет определенной границы, поскольку плотность электронного распределения непрерывно убывает. Поэтому нельзя приписать иону какой-то характерный для него размер. Кажущийся радиус иона зависит от того, какое физическое свойство рассматривается, и будет различным для разных свойств. Нас интересуют такие ионные радиусы, чтобы сумма двух радиусов ( если необходимо, с некоторыми поправками) равнялась равновесному расстоянию между соответствующими соприкасающимися ионами в кристалле. Как будет показано ниже, равновесное расстояние между двумя ионами определяется не только характером распределения электронов в ионах, но также и структурой кристалла и отношением радиусов катиона и аниона. В качестве стандартных кристаллов мы выбираем кристаллы со структурой хлористого натрия, с отношением радиусов катиона и аниона равным около 0 75 и примерно с такой же степенью ионного характера связей, как в галогенидах щелочных металлов. [53]
Во многих системах ( например, W-N, Мо-N, U-N, Th-N) структура типа хлористого натрия ограничена лишь узкими пределами изменений состава. Вне этих пределов имеет место другая структура. Аналогичные условия справедливы и для нитридов элементов с атомными радиусами ниже 1 29 А, например нитридов железа. Они образуют обширную группу метастабильных структур. Американская ассоциация по испытанию материалов ( ASTM) указывает, что в системе Fe-N имеется не менее 12 различных видов структуры. Состав нитридов внедрения может изменяться в широких пределах; все они имеют металлический характер. Структура хлористого натрия образуется лишь тогда, когда состав нитрида отвечает формуле CrN. Хотя по внешнему виду нитрид хрома напоминает металл, его электронная проводимость невелика. [54]
Кроме того, абсолютные значения радиусов таковы, что их суммы равны межионным расстояниям в стандартных кристаллах. Таким путем можно получить радиусы всех ионов с конфигурациями гелия, неона, аргона, криптона и ксенона. Эти радиусы, строго говоря, передают относительные размеры внешних электронных оболочек ионов по сравнению с соответствующими размерами ионов щелочных металлов и галоидов. Эти радиусы имеют следующий смысл. Если бы в стандартном кристалле ( со структурой хлористого натрия), содержащем один из этих катионов с зарядом ze и один из этих анионов с зарядом - ze, кулоновские силы притяжения и отталкивания имели величину, соответствующую зарядам - - е и - е ( как если бы ионы были одновалентными), а специфические силы отталкивания сохранили свою реальную величину, то равновесное межионное расстояние было бы равно сумме этих радиусов. [55]
Для соединений металлов с неметаллами состава 1: 1 известны три различные структуры - структура хлористого цезия с координационным числом восемь, структура хлористого натрия с координационным числом шесть и структура сульфида цинка с координационным числом четыре. Представляет интерес вопрос о том, какая из этих структур наиболее вероятна в каждом конкретном случае. Если предполагать, что соединение - ионное, то наиболее существенным фактором, определяющим структуру, является отношение радиуса аниона к радиусу катиона. Естественно предположить, что стабильность максимальна, если анионы соприкасаются с катионами, а не друг с другом. При ином положении отталкивание между анионами может перевесить притяжение между анионами и катионами. Предположим теперь, что соль АХ имеет структуру хлористого цезия, в которой выполняются сформулированные выше условия и размер катионов А постепенно уменьшается. Окружающие анионы X подходят все ближе друг к другу и наконец начинают соприкасаться. При таком положении весьма вероятно изменение структуры с переходом в структуру с меньшим координационным числом - структуру хлористого натрия. [56]
Два соединения изоморфны, если их молекулы, атомы или ионы настолько сходны по форме и относительным размерам, что они могут образовать кристаллическую решетку. Так, например, большинство переходных металлов первого переходного периода образуют изоморфные сульфаты MSO4 7H2O, так как радиусы ионов М2 примерно одинаковы. Далее, известны квасцы M M ( SO4) 2 12Н2О, где М - одновалентный катион типа калия, рубидия или аммония, а М - трехвалентный катион. В такие кристаллы может входить почти любой трехвалентный катион, но известны лишь немногие квасцы, содержащие в качестве одновалентного катиона натрий, вероятно потому, что натрий слишком мал для обеспечения достаточной устойчивости типичной структуры квасцов. Поскольку наиболее важным фактором являются соотношения между формами и размерами, изоморфны некоторые пары веществ, химически совершенно не сходных. С другой стороны, химическое сходство отнюдь не обязательно должно сопровождаться одинаковыми кристаллическими решетками и изоморфизмом. Так, например, бромистое серебро не изоморфно с обычной формой йодистого серебра. AgBr имеет структуру хлористого натрия с координационным числом шесть, тогда как вследствие меньшего отношения ГА / ГХ Agl обычно имеет структуру вурцита координационным числом четыре. [57]
Страницы: 1 2 3 4