Структура - бензол
Cтраница 3
Как отмечалось ранее, в настоящее время структура бензола представляется в виде плоского кольца, состоящего из шести углеродных атомов с орбитами тг-электронов, расположенными выше и ниже плоскости. Таким образом, ароматическое ядро представляет собой структуру, сравнительно богатую электронами. Эта структура, как таковая, особенно чувствительна к воздействию электрофильных реагентов, несколько менее к воздействию свободных радикалов и наименее чувствительна к воздействию нуклеофилъных реагентов. Действительно, известно очень мало реакций замощения нуклеофильными реагентами простых ароматических углеводородов. [31]
Стремление к созданию характерной для этих циклов структуры бензола с внутренним л-электронньш секстетом является, таким образом, причиной бензолоподобности некоторых б - и 5-членных циклических систем. [32]
Опыты могут служить для постановки вопроса о структуре бензола, так как при ненасыщенности он не дает типичных реакций для непредельности. [33]
Уже отмечалось, что современное представление о структуре бензола ведет к картине, в которой углеродный скелет представляет собой правильный шестиугольник, который содержит орбиты гг-электронов, перпендикулярных к плоской поверхности плоского кольца. Эти тг-электроны определяют необычайную стойкость и другие свойства ароматической системы. [34]
Одна из главных проблем фундаментальной органической химии связана со структурой бензола. [35]
Одна из главных проблем органической химии всегда была свя-зана со структурой бензола. [36]
Так как свойства бензола отличны от свойств ненасыщенных углеводородов, то структура бензола не могла быть выведена по аналогии с этими соединениями. [37]
В конкретном приложении сказанное означает, например, что кекулевская трактовка структуры бензола, понятая в буквальном смысле, не совместима с квантовомеханическими электронными моделями, созданными для описания конкретных молекулярных структур с определенными энергиями. Перераспределение химических связей во времени связано с изменением состояния соответствующих электронов, о котором ничего нельзя сказать, если энергия постоянна и определенна. [38]
Следующий важный случай относится к взаимопревращению бензола и бициклогексадиена, имеющего структуру дыоаровского бензола, но геометрию, сильно отличающуюся от геометрии бензола. [39]
Здесь лишь приводятся некоторые дополнения и уточнения о химической связи и структуре бензола и других ароматических молекул. [40]
Представления о связи между соседними атомами за счет пары электронов плохо объясняют структуру бензола. Все негибридизованные р2 - орбитали параллельны друг другу и перпендикулярны плоскости молекулы. Если межатомные расстояния в бензоле были бы неодинаковы, то можно было предположить, что связь образуется преимущественно путем л-связыва-ния р-орбитали лишь с одним из соседних атомов углерода. Однако поскольку все расстояния С-С равны 1 39А, то каждая орбиталь должна быть в равной степени связана с орбиталями каждого из соседних атомов углерода. Согласно теории валентных схем, представление о паре электронов сохраняется, однако считают, что молекула бензола является резонансным гибридом двух канонических структур. [41]
В дальнейшем выяснилось, что молекулы таких соединений имеют кольчатые структуры, подобные структуре бензола. [42]
Это объясняется тем, что сопряженные двойные замкнутые друг на друга связи в шестиугольной структуре бензола, а значит, и пи-электроны этих связей вступают при переходе в хиноидную форму в более тесное взаимодействие с остальной частью молекулы. [43]
Штарк и Штейбинг отмечают исключительно малую интенсивность свечения растворов флороглюцина, объясняют это отсутствием в флороглюцине структуры бензола и связывают это со склонностью флороглюцина реагировать как трикотон. [44]
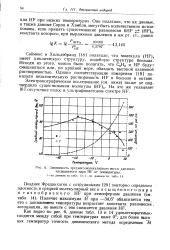 |
Зависимость среднего молекулярного веса и давления насыщенного пара HF от температуры. [45] |
Страницы: 1 2 3 4