Структура - пирит
Cтраница 1
Структура пирита - типа NaCl, но место Na занимают атомы железа, а место С1 - спаренные атомы серы. Кристаллы пирита находятся в друзовых пустотах и в виде пор-фиробластов в различных породах. Часто они выглядят однородными, но А. Ф. Бушмакин, изучая порфиробласты этого минерала из глинисто-кварцевых сланцев, путем травления HNO3 выявил в них реликты структуры горной породы, в которой образовались индивиды пирита. [1]
 |
Элементарная ячейка структур. а СоТе ( структура. [2] |
Структуры пиритов и марказита, названные в соответствии с двумя формами FeS2, имеют совершенно другой вид. Они содержат дискретные группы S2, в которых связи гомеополярны, а расстояние S-S равно 2 10 А. [3]
Структура пирита с группами S2 уже была рассмотрена ранее, и в этом разделе будут описаны полисульфиды лишь с более длинными цепями из атомов S. При описании таких цепей в разд. [4]
Структура пирита с группами S, уже была рассмотрена ранее, и в этом разделе будут описаны полисульфиды лишь с более длинными цепями из атомов S. При описании таких цепей в разд. [5]
Для структуры пирита характерны дисульфидные группы S. [6]
Ситуация здесь аналогична структуре пирита FeS2, в котором радикалы S2 также ориентированы к металлу центром гантели. [7]
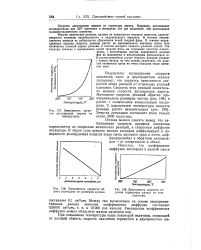 |
Зависимость скорости диссоциации пирита от температуры.| Зависимость скорости обжига колчедана от размеров кусков.| Зависимость скорости горения сернистого железа от температуры. [8] |
Скорость диссоциации зависит от структуры пирита. Например, диссоциация монокристалла при 525 протекает в несколько сот раз медленнее, чем диссоциация поликристаллических агрегатов. [9]
Так, например, в структуре пирита ( рис. 176) узел решетки удобно бывает расположить в середине промежутка между атомами серы. [10]
Эти данные не согласуются с работой [476], в которой указывается на существование RhS2 со структурой пирита. [11]
При составлении таблицы ковалентных радиусов было отмечено4, что расстояние Мп-S в гауерите MnSg ( со структурой пирита) необычайно велико. Впоследствии эта величина была подтвержденаs, и рентгенографическое исследование диселенида марганца и дителяурида марганца6, которые также имеют структуру пирита, привело к подобным же большим межатомным расстояниям. [12]
Кроме того, существуют соединения, содержащие группы As-S, As-As или Р - Р вместо S-S; они имеют структуру пирита или очень близкую структуру. [13]
Сокращенные обозначения кристаллографической структуры: D - тетраэдрическая ( алмаз); Н - гексагональная; N - кубическая ( NaCI); О - оргоромбическая; Р - структура пирита ( серного колчедана); Rli - ромбоэдрическая; Т - тетрагональная; W - структура вуртцига; Z - структура цинковой обманки. [14]
Если перейти к соединениям МО, и MS2, то мы найдем, что многие двуокиси являются ионными, но ионных дисульфидов не существует, так как ион S2 - не может существовать вблизи ионов М4 Вместо ионных структур дисульфиды кристаллизуются в слоистых решетках или в решетке, принадлежащей к очень интересному типу структур пирита ( см. стр. Обзор эмпирических формул различных окислов и сульфидов переходных металлов показывает, что в некоторых случаях существует окись АОЛ, а аналогичного сульфида А5Л не существует. В других случаях установлено существование данного сульфида, а соответствующий ему окисел не выделен. Эти факты можно связать со свойствами кислорода и серы следующим путем. [15]
Страницы: 1 2