Структура - пора - адсорбент
Cтраница 2
Длительность процесса адсорбции зависит от природы адсорбента ( поглотителя) и адоорбива ( поглощаемого вещества); от величины удельной поверхности и структуры пор адсорбента; от температуры и парциального давления поглощаемых газов, На обычных установках периодячеокого действия ( происходит чередование оледуицих циклов: поглощение адоорбентаки углеводородов и елати ив гавов, отгонка поглощенных гаеов, сушка адсорбенте, охлаждение адсорбента) шкл адсорбции продол ите-дев и1 дохади до iO - i2 часов, Во ВНИЛГазе разработан процесс Овр адсорбции, пр адназначенннй для извлечения vie адвиоатКЫх месторрадении жидких углеводородов и влаги. [16]
В уравнениях ( 1) и ( 2) а - величина адсорбции, ммоль / г; W0 - предельный объем адсорбционного пространства, см3 / г; В - константа, зависящая от структуры пор адсорбента, град 2; Т - температура, К; р - коэффициент аффинности; Р - парциальное давление адсорбата, ат; Ркр - критическое давление адсорбата, ат; т - приведенная температура: т 71 / Гжр, где Tgp - критическая температура адсорбата, К; а0, аг - коэффициенты прямолинейной корреляции. [17]
Капиллярная конденсация описывается обычно уравнениями Томсона, применимыми для круглых цилиндрических капилляров. В действительности, структура пор адсорбентов весьма сложна и не отвечает представлению о таких капиллярах. Кистлер, Фишер и Фримен в 1943 г. сделали важную попытку обобщить представления о капиллярной конденсации паров на поры любой формы при помощи уравнения Вольцмана и получили формулу для определения поверхности адсорбционной пленки s, на которой начинается капиллярная конденсация. [18]
В связи с этим иногда высказывают мнение, что определение удельной поверхности возможно только для непористых веществ. Однако исследования влияния структуры пор адсорбентов на их адсорбционные свойства позволили устранить в значительной мере помехи по определению удельной поверхности, вносимые пористой структурой. [19]
Если зависимость величины предельной адсорбции от структуры пор адсорбента подробно исследовалась в работах [3-9, 14], влияние природы поверхности адсорбента на адсорбцию из растворов не подвергалось еще систематическому изучению. Для раздельного изучения факторов представляют особый интерес исследования адсорбции из растворов, с одной стороны, на пористых и непористых адсорбентах с одинаковой природной поверхностью, с другой стороны, на непористых адсорбентах с различной природной поверхности. Для гидрофобных адсорбентов сопоставление изотерм адсорбции некоторых органических веществ из водных растворов на угле и непористой саже было проведено в работе [11], однако при этих исследованиях не учитывалось различие в природе поверхности использованных адсорбентов, соответствующих данных в работе не приведено. [20]
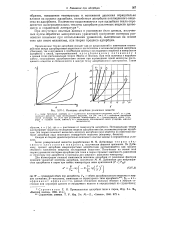
Применению метода капиллярной конденсации пара для изучения структуры пор органических адсорбентов обычно препятствует их набухание. Чтобы избежать набухания, следует применять адсорбаты, межмолекулярные взаимодействия которых с матрицей полимера слабые. Сравнение изотерм сорбции и десорбции на пористых полимерах адсорбатов разной природы ( рис. 6.3) показало, что в паре перфтор-н-октана, в отличие от метанола, набухания полимеров не происходит. Изотерма адсорбции этого пара в начальной области полностью обратима. При более высоких относительных давлениях пара р / ро наблюдается четкий капиллярно-конденсационный гистерезис, как в случае неорганических адсорбентов с жестким СКелетОМ ( СМ. [21]
Кг - коэффициент распределения, представляющий меру доступности объема пор адсорбента для данного компонента. Коэффициент распределения Кг представляет важную характеристику в ЖСХ; его величина определяется главным образом структурой пор адсорбента и размерами макромолекул полимера. [22]
Адсорбционный метод разделения газовых смесей основан на избирательном поглощении углеводородов твердыми сорбентами, хорошо поглощающими ( адсорбирующими) высшие углеводороды и практически не адсорбирующими основной разбавляющий компонент - метан. Величина адсорбции газа или паров зависит от природы поглощающего вещества ( адсорбента) и поглощаемого вещества ( адсорбтива), величины удельной поверхности и структуры пор адсорбента, парциального давления поглощаемых паров или газов и температуры. [23]
 |
Схема менисков при конденсации пара в цилиндрическом ( а и коническом ( б капиллярах.| Кривая распределения пор адсорбента по размерам ( структурная кривая. [24] |
Тем более это относится к гетеропористым адсорбентам, обычно встречающимся в практике. В данном случае исследование зависимости х от р, а следовательно от R, в области капиллярной конденсации имеет огромное практическое значение, ибо позволяет дать характеристику структуры пор адсорбента, построить интегральную кривую распределения пор по размерам. [25]
Ограниченность рассмотренной теории, как теории адсорбции, заключается прежде всего в том, что она применима не ко всей изотерме, а лишь к ее участку - петле гистерезиса. Несмотря на это, исследование зависимости V от р, а следовательно, и от г, в области капиллярной конденсации имеет огромное практическое значение, так как позволяет дать характеристику структуры пор адсорбента и построить дифференциальную кривую их распределения по размерам. [26]
Адсорбция газов при температуре выше критической, повидимому, протекает мономолекулярно. При мономолекулярной адсорбции структура пор адсорбента имеет значение лишь в том случае, если значительная часть поверхности приходится на долю пор, диаметр которых не превышает одного или двух диаметров молекул адсорбируемого вещества. Теплота адсорбции в таких тонких порах выше, чем на плоской поверхности, так как молекулы газа испытывают притяжение не только с одной стороны. Это приводит к повышению адсорбции при низких давлениях. Если же поры слишком тонки, то молекулы совсем не могут в них проникнуть, и количество адсорбированного вещества заметно снижается, а иногда адсорбция оказывается совсем невозможной. Адсорбенты с очень тонкими порами можно рассматривать как молекулярные сита; в их поры могут проникать молекулы лишь очень небольших размеров. Более крупньш молекулам самые тонкие поры недоступны. Мак-Бэнр ] называет это явление п е р-сорбцией. [27]
 |
Зависимость lg VR для некоторых конденсированных ароматических углеводородов от числа атомов углерода в молекуле п. [28] |
Селективность адсорбента и абсолютные ( в расчете на единицу поверхности) величины удерживаемых объемов в основном зависят от химической природы поверхности и элюента. Влияние этих факторов рассмотрено в разд. Эффективность же адсорбционной колонны зависит в значительной степени от размера и формы зерен и структуры пор адсорбента. Влияние этих факторов рассмотрено в гл. Здесь мы рассмотрим влияние удельной поверхности адсорбента на удерживаемые объемы. [29]
 |
Изотермы адсорбции различных веществ. [30] |
Страницы: 1 2 3