Структура - рутил
Cтраница 3
Структура силлиманита: сходна со структурой рутила TiCb, в основе которой лежит гексагональная плотнейшая упаковка. В отличие от рутила, в структуре силлиманита лишний атом кислорода, соединяющий 2 тетраэдра, располагается в октаэдрических пустотах, остающихся в рутиле пустыми. Тот же характер структуры и у тортвейтита. Связующий атом кислорода группы [ SizOy ] занимает центр октаэдра. [31]
Стишовит очень интересен, поскольку имеет структуру рутила с октаэдрической координацией кремния. Во всех других формах двуокиси кремния каждый атом кремния находится в тетраэдри-ческом окружении, состоящем из четырех атомов кислорода. [32]
Обычная темно-бордовая модификация этого оксида имеет структуру рутила, среднее расстояние РЬ-О в октаэдрах РЬО6 2 18 А. При температуре 300 С и давлении 40 кбар эта модификация превращается в черную ромбическую модификацию, структура которой описана в гл. [34]
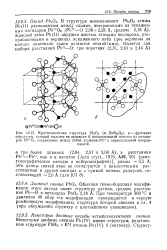
Связь октаэдров [ ТЮ6 ] в структуре рутила в проекции вдоль оси с приведена на рис. 23.8, а, где значение z - координаты окта эдров ( г 0 и YZ) показано при помощи различной штриховки При этом в направлении оси с октаэдры располагаются один нал другим и соединяются через общие ребра. [35]
Связь октаэдров [ TiO6 ] в структуре рутила в проекции вдоль оси с приведена на рис. 23.8, а, где значение z - координаты октаэдров ( z 0 и 1 / а) показано при помощи различной штриховки При этом в направлении оси с октаэдры располагаются один над другим и соединяются через общие ребра. [36]
Гомологические серии оксидов, структурно родственных структуре рутила. Ванадий и титан образуют серии оксидов общего состава М О2п 1 со структурами, родственными структуре рутила. Блоки рутилоподобной структуры толщиной в п октаэдров, но бесконечно протяженные в двух других измерениях, сочленены между собой по плоскостям сдвига. Эти структуры можно геометрически вывести из структуры рутила удалением части атомов кислорода из определенных плоскостей и последующим смещением рутильных блоков таким образом, чтобы восстановить октаэдрическую координацию атомов металла. Эта операция приводит к соединению разных блоков по граням определенных пар октаэдров ( в дополнение к связыванию по вершинам и ребрам в самих рутильных блоках), как в структуре типа корунда ( разд. При этом возникают структуры, в которых определенные октаэдры соединены по ребрам. Литература об оксидах Ti ( 4 n 9) и V ( 3 п 8) приведена в гл. [37]
Двуокиси Sn02 и РЬО2 кристаллизуются в структуре рутила и должны рассматриваться преимущественно как кристаллы. Свинец не образует дисульфида, a SnS2 имеет слоистую структуру йодистого кадмия, в которой атомы олова имеют шесть октаэдрически расположенных соседних атомов серы. [38]
Хотя координационный полиэдр иона металла в структуре тетрагонального рутила близок к правильному октаэдру, при точном определении расстояний М - О в них обнаруживаются небольшие различия. Например, в структуре ТЮ2 [3] четыре расстояния Ti-О равны 1 944 ( 4) А и два расстояния - 1 988 ( 6) А; в структуре RuC2 [4] есть четыре расстояния Ru-О, равные 1 917 ( 8) А, и два-1 999 ( 8) А. [39]
Имеется ряд дифторидов переходных элементов со структурой рутила, например дифторид марганца, дифторид железа, дифторид кобальта, дифторид никеля. [40]
При этом получают грубодисперсную двуокись со структурой рутила. [41]
& % 1 0 также со структурой рутила; в промежуточной области концентраций эти две рутзлъше фазы сосуществуют. [42]
ТсОг, как и MnOs, имеет структуру искаженного рутила. [43]
Кроме общеизвестного ферромагнитного оксида ОО2 ( со структурой рутила) были синтезированы CrF4 и СгВг4; однако в настоящее время их строение еще неизвестно. Из сопоставления формы группировок в 5г2СгО4 и в CrCX ( табл. 27.3) видно, что анионы СгО44 в первом из этих соединений искажены значительно больше, чем тетраэдры во втором. [44]
 |
Соотношения между структурами с гексагональной плотнейшей упаковкой. [45] |
Страницы: 1 2 3 4 5