Структура - рутил
Cтраница 4
Например, структуры MgU04 и ZnSb2O6 оказываются родственными структуре рутила. [46]
 |
Зависимость устойчивости. [47] |
Полученные значения свидетельствуют о возможной кристаллизации SnO2 в структуре рутила. Выводы о структуре SrF2 и SnO2 подтверждаются экспериментально. [48]
При 797 С а-форма переходит в модификацию с неискаженной структурой рутила и металлич. Методом хим. транспортных р-ций из МЬС15 или КЬ3О7С1 получен р - МЪО2 ( отношение О: МЬ 1 990 - 1 988) с иным типом искажения структуры рутила; вероятно, метастабилен. Получают МЬО2 спеканием смеси МЬ2О5 и ЫЬ в вакууме при 1130 С или как промежут. [49]
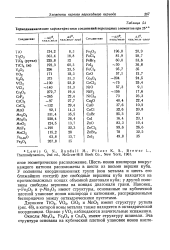 |
Термодинамические характеристики соединений переходных элементов при 25 а. [50] |
Двуокиси TiO2, VO2, СгО2 и МпО2 имеют структуру рутила ( рис. 48), в которой ионы металла также находятся в октаэдрической координации. Однако у VO2 наблюдаются значительные искажения. [51]
Двуокись титана, полученная при высоких температурах, имеет структуру рутила, при более низких - структуру анатаза. Очень устойчива к действию различных реагентов. В кислотах, кроме плавиковой и серной, не растворяется. Серная кислота медленно растворяет двуокись, прокаленную ниже 800 и имеющую структуру анатаза. Действие на нее водных растворов щелочей ничтожно. [52]
 |
Структура флюорита CaF2.| Структура рутила ТЮ2. [53] |
Следует добавить, что в противоположность трем уже рассмотренным структурам структура рутила относится к тетрагональной системе. [54]
Однако необходимо иметь в виду, что из-за смещения блоков структуры рутила часть получающихся узлов ячейки оказывается в TisO9 вакантной, поэтому если брать узлы, лежащие вне ячейки Ti5Og, то могут получаться координаты этих вакантных узлов. Этого не происходит, если узлы обеих ячеек совпадают. [55]
Согласно Джонсону и Уэйлу, добавление окиси циркония повышает восприимчивость структуры рутила к таким ионам с более высокой валентностью. В полупроводящих кристаллах образуются ионы Тг3, которые можно рассматривать как ионы Ti4 с прилипшими электронами. Последние особенно легко высвобождаются и вызывают электронную проводимость. [56]
 |
Структура кристалла флюорита CaFj ( стереоскопическое изображение. [57] |
Аналогичные расчеты показывают, что при постоянном расстоянии между катионом и анионом структура рутила ( координационное число 6) на 8 % устойчивее структуры кварца ( координационное число 4), а структура флюорита ( координационное число 8) на 5 % устойчивее структуры рутила. [58]
 |
Три способа изображения молекулы Р4О 0. [59] |
Если одни структуры характерны только для связей определенного типа ( например, структура рутила для преимущественно ионных оксидов и фторидов АХ2), то другие простые структуры АтХ могут реализоваться при разных типах связи. [60]
Страницы: 1 2 3 4 5