Структура - спирт
Cтраница 2
С помощью спектров ЯМР ( Н1) определена структура бицик-лических спиртов на основе б-метилпентахлорциклопентадиена, пента - и тетрахлорциклопентадиенов и аллилового спирта. Показано, что реакции 5-метилпентахлорциклопентадиена и пентахлорцик-лолентадиена с аллиловым спиртом проходят стереоспецифичнс, образуется только эндо-аддукт, имеющий син-анти-изомеры. При использовании тетрахлорциклопентадиена образуется смесь экзо-эндо-изомеров. [16]
С помощью спектров ЯМР ( Н1) определена структура бицик-лических спиртов на основе 5-метилпентахлорциклопентадиена, пента - и тетра. Показано, что реакции 5-метилпентахлорциклопентадиена и пентахлорцик-лолентадиена с аллиловым спиртом проходят стереоспецифичнс, образуется только эндо-аддукт, имеющий син-анти-изомеры. При использовании тетрахлорциклопентадиена образуется смесь экзо-вндо-изомеров. [17]
Это, несомненно, связано с меньшей упорядоченностью структуры спиртов по сравнению со структурой воды. [18]
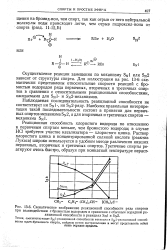 |
Схематическое изображение реакционной способности ряда спиртов при взаимодействии с бромистым водородом в сравнении с обычным порядком реакционной способности в реакциях SN. и 5м2. [19] |
Осуществление реакции замещения по механизму SN1 или зависит от структуры спирта. Для иллюстрации на рис. 13 - 6 схематически представлены относительные скорости реакций с бромистым водородом ряда первичных, вторичных и третичных спиртов в сравнении с относительными реакционными способностями, ожидаемыми для SN1 - и 5к2 - механизмов. [20]
Алкоксихлорсиланы и тетраалкоксисиланы образуются в различном соотношении в зависимости от структуры спирта и молярного соотношения спирта к тетрахлорсилану. [21]
На рис. П-47 показано измерение окисляемости kpk 2 в зависимости от структуры спирта. [22]
Легкость переэтерификации зависит как от строения диал-килфосфита, так и от структуры спирта, вводимого в реакцию. Так, диэтилфосфит переэте-рифицируется дециловым спиртом при 160 - 170 С, ди - ( ( 5-хлор-этил) - фосфит при 140 - 150 С, а ди - ( р-фторэтил) - фосфит прн 120 - 130 СС. Реакция протекает при температуре около 100 С без отгонки фенола, причем внесение катализатора не изменяет скорости процесса. Выходы диалкилфосфитов почти количественные. [23]
Легкость переэтерификации зависит как от строения диал-килфосфита, так и от структуры спирта, вводимого в реакцию. Так, диэтилфосфит переэте-рифицируется дециловым спиртом при 160 - 170 С, ди - ( р-хлор-этил) - фосфит при 140 - 150 С, а ди - ( 3-фторэтил) - фосфит при 120 - 130 С. Реакция протекает при температуре около 100 С без отгонки фенола, причем внесение катализатора не изменяет скорости процесса. Выходы диалкилфосфитов почти количественные. [24]
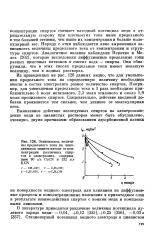 |
Зависимость величины предельного тока на неподвижном медном катоде от концентрации различных спиртов в электролите, содержащем 90 г / л CuCN и 132 г / л KCN. [25] |
Наряду с этим наблюдается явно выраженная зависимость величины предельного тока от концентрации и структуры спиртов. Аналогичное явление наблюдали Перачио и Ме-лох [202], которые исследовали диффузионные предельные токи разных щелочных катионов в смесях вода - спирты. Они обнаружили, что в этих смесях предельные токи имеют меньшую величину, чем в водных растворах. [26]
Эта область сравнительно велика благодаря тому, что молекулы воды могут легко встраиваться в структуру спирта. Для области больших концентраций спирта характерна относительно плавная зависимость от состава термодинамических свойств и парциальных величин, их значения здесь в меньшей степени зависят от температуры, чем в области больших концентраций воды. Последнее обстоятельство связано с тем, что изменения температуры в значительно меньшей степени влияют на структуру чистых спиртов, чем на структуру воды. В качестве заключения к данному обзору следует сказать, что изучение термодинамических свойств спирто-водных растворов еще далеко не закончено. Дальнейшая работа в этой области, по-видимому, должна быть направлена на детализацию термодинамических свойств спирто-водных растворов в более широком интервале температур. [27]
Из данных табл. 2 можно сделать вывод, что величина Е зависит не только1 от структуры спиртов, но и в значительной степени от природы и генезиса АЬОз-катализатора. [28]
Физико-химические [43, 44] и топологические [48] методы были использованы для исследования зависимости степени ингибирования гидроксилирования анилина от структуры спиртов. В табл. 3 представлены совместно с экспериментальными данными, взятыми из работы Коэна и Маннеринга [43], величины plC50, IC0, SIC, и С1С2 для серии из 20 спиртов. [29]
В том же 1864 г. в поправке к статье о псевдобутильном алкоголе [82] А. М. Бутлеров снова обсуждает теоретически допустимые структуры спиртов С5НпОН и приходит к заключению, что всего возможно 8 структурно-изомерных спиртов этого состава. [30]
Страницы: 1 2 3 4