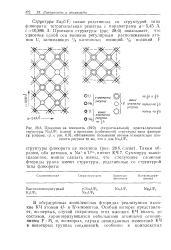
Структура - тип - флюорит
Cтраница 1
 |
Структура флюорита ( CaF2. [1] |
Структура типа флюорита, в которой позиции катионов заняты анионами, а позиции анионов - катионами, называется анти-флюоритовой. [2]
 |
Структура FesAl. [3] |
Структуры типа флюорита, дефектные по катионам, по-видимому, встречаются редко. [4]
Для TiD2 структура типа флюорита подтверждена нейт-ронографически. Следует подчеркнуть, что гидриды, которым ранее приписывали формулы Zr2H и Zr4H, не являются индивидуальными соединениями, а соответствуют произвольно выбранным точкам на фазовой диаграмме. Тот факт, что в тетрагональных гидридах Zr и Hf ( состава МН2) расположение атомов металла менее симметрично, чем в структурах с дефектами, указывает на важную роль в этих структурах связей металл - водород. [5]
Существует борид бериллия Ве2В со структурой типа флюорита и многочисленные борнды М2В со структурой СиАЬ, которая описана в разд. Соседние слои повернуты друг относительно друга на 45, а атомы В находятся в центрах антипризм, образованных двумя квадратными группами из соседних слоев. В структуре Fe2B атом В координирует восемь атомов Fe на расстоянии 2 18 А и еще два атома В на расстоянии 2 12 А ( но это не связь В-В. [6]
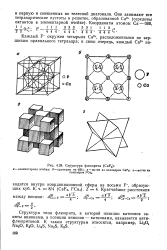
Структура NazUF7 также родственна со структурой типа флюорита: тетрагональная решетка с параметрами а 5 45 А, с10 896 А. Проекция структуры ( рис. 28.6) показывает, что удвоение одной оси вызвано регулярным расположением атомов U, занимающих / 4 катионных позиций. [8]
Кубическая и тетрагональная формы ZrC2 имеют структуру типа флюорита CaF2, а моноклинная - деформированную решетку, промежуточную между флюоритом и рутилом. [9]
Высокотемпературная кубическая фаза диоксида циркония, имеющая структуру типа флюорита ( рис. 7.18), становится стабильной прп комнатной температуре благодаря образованию твердых растворов с CaO, Y203 п др. Такой стабилизированный диоксид циркония при высоких температурах имеет высокую О2 - ионную проводимость, появляющеюся в результате накопления кислородных вакансий, компенсирующих при образовании твердого раствора недостаток положительного заряда катионов. [10]
Они имеют ромбоэдрические решетки, близкие к структуре типа флюорита. Вдоль оси с эти октаэдры чередуются с октаэдрами, не содержащими атомов урана. [11]
 |
Проекция крпсталлплеской структуры f - a2UF6. [12] |
Структура Y-N UFe представляет собой слегка искаженную сверхструктуру на основе структуры типа флюорита, в которой оба сорта положительных ионов имеют восьмерную координацию ( рис. 28.5) и размещены упорядочение. [13]
Покажите, что при удалении необходимого числа катионов из кристалла типа криолита он переходит в структуру типа флюорита, соответствующую правильной формуле. Для этого рассмотрите, сколько ионов [ АВв ] 2 - 3 - содержится в каждой элементарной ячейке. [14]
Стабилизация кубического ZrO2 происходит также за счет изоморфных замещений катионами Са2, Y3, Sc3 и др. При этом сохраняется структура типа флюорита, но с образованием кислородных вакансий в тетраэдрических пустотах, образованных катионами. [15]
Страницы: 1 2 3