Структура - жидкая вода
Cтраница 1
 |
Схематическое изображение МОЛекуЛ ВОДЫ. Это ПрИВОДИТ структуры молекул воды К ВОЗНИКНОВенИЮ ВОДОрОД. [1] |
Структура жидкой воды выяснена не столь детально, как структура льда. Для структуры воды было предложено много моделей. [2]
Структура жидкой воды достаточно сложна, а информация, извлекаемая из ее спектра с широкими полосами, весьма ограниченна. Тем не менее метод инфракрасной спектроскопии позволяет установить ряд ее свойств. Это является прямым доказательством того, что структура жидкой воды не искажается под действием вводимых в нее ионов и молекул на расстоянии, большем чем 10 - 30 А. [3]
Структура жидкой воды подобна структуре льда, но расположение молекул в ней менее упорядочено. [4]
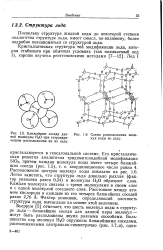 |
Ближайшие соседи данной молекулы Н2О при тетраэдри-ческом расположении их во льду.| Схема расположения молекул воды во льду. [5] |
Поскольку структура жидкой воды до некоторой степени аналогична структуре льда, имеет смысл, по-видимому, более подробно познакомиться со структурой льда. [6]
 |
Структура льда. [7] |
Описанная модель структуры жидкой воды позволяет по-новому оценить и строение водных растворов электролитов, являющихся дисперсионной средой всех ( в том числе неминерализованных) промывочных жидкостей на водной основе. [8]
 |
Схема структуры гидрата воды по Полингу. [9] |
Согласно этой модели, структура жидкой воды представляет собой гидрат воды ( раствор внедрения воды в воде), состоящий из беспорядочной смеси нестабильных каркасов, в полостях которых находятся мономерные молекулы воды. Этот каркас имеет симметрию икосаэдра ( рис. 1.10) и образован двадцатью одной молекулой воды, из которых двадцать расположены в вершинах пентадодекаэдра и каждая из них связана с ближайшими соседями тремя водородными связями. Двадцать первая молекула не образует водородных связей и находится в полости, внутри додекаэдра. Взаимное расположение додекаэдров может быть весьма различным: так, они могут быть соединены между собой водородными связями, или иметь общую пятиугольную грань, или могут соединяться мостиками, образованными цепями молекул воды, соединенных водородными связями. Кроме всего этого, в воде могут присутствовать свободные мономерные молекулы, не образующие водородных связей. Существование цепей и мостиков из молекул воды может также приводить к образованию добавочных полостей еще большего диаметра. [10]
Различные количественные исследования [16, 38, 41, 62, 70, 71] структуры жидкой воды обычно достаточно хорошо объясняют ее термодинамические свойства. Наибольшая трудность обычно возникает при предсказании величины теплоемкости. [11]
 |
Расположение сфер в плотнейшей кубической ( о и гексагональной ( б упаковке. [12] |
Таким образом, особенность структуры жидкой воды проявляется в пространственной сетке водородных связей и наличии в ней пустот, которые могут заполняться молекулами. В связи с этим жидкая вода проявляет особые свойства по сравнению с теми, которые следовало бы ожидать от характера изменений их в ряду сходных соединений Н2О, H2S, HaSe, HaTe. Так, температуры плавления и кипения ее должны были бы быть равными около 173 15 К и 193 15 К соответствен-но вместо 273 15 К и 373 15 К, наблюдаемых на опыте. С указанными особенностями связаны максимальная плотность воды при 277 15 К, высокое значение диэлектрической постоянной и другие свойства. [13]
Представляет особый интерес модель структуры жидкой воды в виде мерцающих кластеров ( рис. 4), состоящих из соединенных водородными связями молекул, плавающих в более или менее свободной воде. Кластеры постоянно существуют в текучей жидкости, непрерывно образуясь и разрушаясь в соответствии со случайными тепловыми изменениями в микроучастках жидкости. Фрэнк и Вин определили время полужизни кластера как 10 - 10 - 1 - ю - 11 с, что соответствует времени релаксационных процессов в воде. [14]
В свою очередь нарушение самосогласованной структуры однородной жидкой воды введением чужих молекул уже в очень малых концентрациях - ( 10 - 9) приводит к изменению характера межмолекулярного взаимодействия в воде и в определенной области малых концентраций может привести к нелинейной зависимости свойств раствора от концентрации растворенного вещества. [15]
Страницы: 1 2 3 4