Структура - галогенид
Cтраница 1
Структуры галогенидов, гидридов, гидроксидов щелочных металлов либо относятся к 2 кубическим формам ( тип NaCl и CsCl), либо обнаруживают деформацию ромбоэдрическую - сульфгидриды, селеногид-риды - или тетрагональную - LiOH. Ромбическая деформация не обнаружена. [1]
Структуры галогенидов можно подразделить на два основных типа: ионные и ковалентные, а последние, в свою очередь, на координационные и псевдомолекулярные - цепные, слоистые. Условной границей между этими двумя типами структур является диагональная граница между металлами и неметаллами. При этом элемент должен быть расположен слева от диагональной границы. При более высоких степенях окисления катионообразователя существуют псевдомолекулярные и молекулярные структуры. [2]
Структуры галогенидов Ag и, в частности, AgJ представляют большой теоретический интерес. [3]
В структуре низших галогенидов ниобия, равно как и других переходных элементов V-VIII групп, большую роль играют связи между атомами металла за счет перекрывания d - или d - гибридных орбиталей. Такие группы атомов металла называют металл-кластерами или кластерами. [4]
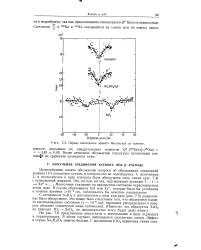 |
Первые наблюдения эффекта Мессбауэра на ксеноне. [5] |
Более детальное обсуждение структуры галогенидов ксенона их сравнение проводятся ниже. [6]
Во многих галогенидах атомы галоидов плотно упакованы ( см. структуры галогенидов, стр. Ионы фтора очень близки по размеру к нонам кислорода, и поэтому эти два иона вместе могут построить плотно упакованную структуру. [7]
Структуры амидов, содержащих анион NH2, имеют большое сходство со структурами галогенидов s - эле-ментов. [8]
 |
Структура молекул хлорида, бромида и иодида алюминия в парообразном состоянии. [9] |
Несмотря на то что его структура не установлена окончательно, весьма вероятно [ по аналогии со структурами других галогенидов, в том числе хлорида железа ( Ш) 1, что решетка хлорида алюминия имеет преимущественно ионный характер, в которой каждый атом алюминия окружен шестью атомами хлора. [10]
Халькогениды сильно электроположительных элементов ( металлов) обычно кристаллизуются с образованием типичных ионных решеток, имеющих структуру, близкую к структуре галогенидов. [11]
Изменение от бесконечной трехмерной связи М - F - М во фторидах до слоев, цепей или молекулярных решеток в других галогенидах должно быть отнесено за счет усиления ко-валентного характера связей между металлом и галоидом. Дальнейшее обсуждение структур галогенидов должно быть отложено до гл. [13]
 |
Структурные типы соединений. [14] |
Соединения щелочных металлов с галогенами и водородом ( A1BVI1) имеют структуру типа каменной соли ( соединения CsGl, CsBr, Csl имеют структуру типа хлористого цезия) и обладают ярко выраженным ионным характером, обусловленным сильной электроположительностью этих металлов и столь же сильной электроотрицательностью галогенов. Таковы должны быть и структуры галогенидов франция. От галогенидов натрия к галогенидам лития увеличивается доля ковалентной связи. Водород с галогенами образует ковалентно-ионные соединения, которые отличаются от ионных соединений и по этому признаку должны быть сильно смещены вправо. Соединения меди с водородом и галогенами относятся к структурным типам сфалерита ( цинковой обманки) и вюртцита. Происхождение соединений AIIIB V с такой структурой обусловлено образованием тетраэдрически направленных связей вследствие разделения четырех пар электронов с антипараллельными спинами между соседними атомами, Образование этих ковалентных структур с полупроводниковыми свойствами соответствует сдвигу меди, серебра и золота вправо относительно лития. Серебро образует с галогенами ионные соединения со структурой типа хлористого натрия. [15]
Страницы: 1 2
