Электронная структура
Cтраница 2
Электронная структура их атомов выражается формулой ( п - l Vis2, где п - номер внешнего слоя, совпадающий с номером периода. При возбуждении атома внешние s - электроны распариваются, поэтому скандий и его аналоги могут проявлять валентность, равную двум. [16]
Электронная структура их атомов выражается формулой ( п - l) d ns2, где п - номер внешнего слоя, совпадающий с номером периода. При возбуждении атома внешние s - электроны распариваются, поэтому скандий и его аналоги могут проявлять валентность, равную двум. [17]
Электронная структура 6d27s 7p, степень окисления 2, 3 и 4, последняя наиболее характерна. [18]
Электронная структура может быть представлена и с помощью электронной формулы. Так как в электронной оболочке атома ванадия ( Z 23) сохраняется расположение электронов, присущее предшествующему благородному газу аргону ( Z18) - Is 2s22p63s23p6, то для краткости в электронной формуле заменяют начальные электроны символом соответствующего благородного газа. [19]
Электронная структура может быть представлена и с помощью электронной формулы. Так как в электронной оболочке атома ванадия ( Z 23) сохраняется расположение электронов, присущее предшествующему благородному газу аргону ( Z 18) - Is22s22p63s23jp6, то для краткости в электронной формуле заменяют начальные электроны символом соответствующего благородного газа. [20]
Электронная структура галогенбешюлов п их поведение в процессе эликтрофнлыюго замощения. [21]
Электронная структура однозначно определяет вообще возможность образования более или менее устойчивой цепи. Обрамляющие группы модифицируют электронную структуру, защищают главную цепь от атаки нуклеофильными или электрофильными агентами и, наконец, определяют характер межцеиных взаимодействий. [22]
Электронные структуры окислов азота приведены ниже. Большинство молекул этих веществ является гибридами резонансных структур, причем на схеме показаны не все существующие структуры; для пятиокиси азота, например, различные одинарные и двойные связи могут меняться местами. [23]
Электронные структуры окислов азота приведены ниже. [24]
Электронная структура для изолированного иона Fe2 должна быть такой, при которой четыре Srf-орбитали должны быть заняты одиночными электронами с параллельными спинами, а одна занята парой электронов. Ион с такой структурой будет иметь магнитный момент, соответствующий параллельно ориентированным спинам четырех неспаренных электронов. Экспериментально установлено, что гидратиро-ванный ион железа ( П) Fe ( H2O) § имеет магнитный момент именно с таким значением, в то время как ион гексацианоферрата ( П) магнитным моментом не обладает. Отсюда можно сделать вывод, что связи в этих двух комплексных ионах различны по своему характеру: в гид-ратированном ионе железа ( II) эти связи, имеющие значительный ионный характер, образованы с использованием 4з - орбитали и трех 4р - ор-биталей, в то время как в ионе гексацианоферрата ( П) орбитали dzsp3 образуют ковалентные связи. Изучение магнитных свойств комплекса очень часто позволяет сделать вывод о природе орбиталей связи, использованных атомами данного металла. [25]
Электронные структуры железа, кобальта, никеля и платиновых металлов указаны в табл. 19.1; эти структуры соответствуют энергетическим уровням, приведенным на рис. 5.6. Следует отметить, что каждый из рассматриваемых атомов имеет два внешних электрона: в случае железа, кобальта и никеля это электроны на 4-орбитали, для рутения, родия и палладия - на Ss-орбитали; для осмия, иридия и платины - на бз-орбитали. [26]
Электронные структуры актинидов до сих пор не установлены достаточно точно. В настоящее время можно считать установленным, что 5 / - электроны у тория отсутствуют. [27]
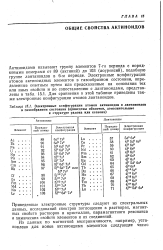 |
Электронны конфигурации атомов актиноидов и лантаноидов. [28] |
Приведенные электронные структуры следуют из спектральных данных, исследований спектров поглощения в растворах, магнитных свойств растворов и кристаллов, парамагнитного резонанса и химических свойств элементов и их соединений. [29]
Электронная структура бериллия - Is22s2, и 25-под-уровень заполнен целиком. [30]
Страницы: 1 2 3 4