Кристаллическая структура - льд
Cтраница 1
Кристаллическая структура льда относится к тридимитной с водородными связями между своеобразно расположенными парными электронами молекул воды. По мере повышения температуры от 273 К до 277 К лед превращается в воду и в ней постепенно образуется другая структура, в которой тетраэдры из молекул воды располагаются не в виде слоев, а по направлениям ориентации водородных связей. [1]
Кристаллическая структура льда была предметом многочисленных исследований и вызывала много споров в течение трех десятилетий. Тем не менее остается ряд невыясненных вопросов, требующих дальнейшего изучения. Еще позднее появились две превосходные статьи - Лонсдейл [ 1257а ] и Оустона [ 1561 в ] - посвященные современным представлениям о кристаллической структуре льда. В связи с наличием перечисленных основательных обзорных работ здесь нет необходимости подробно обсуждать кристаллические свойства воды. [2]
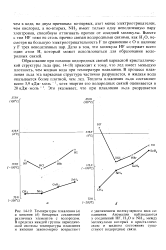 |
Температуры плавления ( а и кипения ( б бинарных соединений различных элементов с водородом. В пределах каждой группы периодической системы температуры плавления и кипения закономерно возрастают. [3] |
Образование при помощи водородных связей каркасной кристаллической структуры льда ( рис. 14 - 18) приводит к тому, что лед имеет меньшую плотность, чем жидкая вода при температуре плавления. В процессе плавления льда эта каркасная структура частично разрушается, и жидкая вода оказывается более плотной, чем лед. [4]
 |
Структура флуорита.| Структура рутила. [5] |
Как видно из рис. 1.87, кристаллическая структура льда имеет полости, что обусловливает его низкую плотность, меньшую плотности воды. Полости в кристаллической решетке льда могут заполняться другими молекулами, например СН4, H2S, одноатомными молекулами благородных газов, в результате чего образуюхся своеобразные химические соединения. Соединения, получаемые в результате включения в полости кристаллической решетки молекул других соединений, называют клатратами. [6]
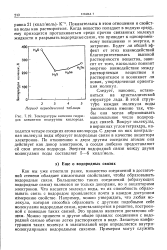 |
Температуры кипения гидри. [7] |
Следует, наконец, остановиться на кристаллической структуре льда. [8]
Какую роль играют водородные связи в образовании кристаллической структуры льда. Какое влияние они оказывают на свойства льда. [9]
Это приводит к тому, что в кристаллической структуре льда каждый атом кислорода окружен четырьмя атомами водорода: двумя связанными ко-валентно и двумя мостиковыми. В результате образуется тетраэдри-ческая структура с необычно рыхлой упаковкой частиц ( рис. В. При плавлении льда часть водородных связей разрушается, и в жидкости находятся в динамическом равновесии молекулярные ассоциаты, содержащие до 100 молекул воды, представляющие собой осколки структуры льда. Отдельные молекулы воды могут путем быстрого обмена ( - 10-и с) присоединяться к ассо-циату или отщепляться от него. [10]
Согласно этой теории, регулярно расположенные пустоты в кристаллической структуре льда, имеющие размеры, большие, чем диаметр молекулы Н2О, не остаются пустыми после плавления, а вследствие большой подвижности молекул в воде могут заполняться отдельными молекулами. Учитывая, что в этих пустотах потенциальная энергия имеет локальный минимум, молекулы воды, попадающие в эти пустоты, остаются там в течение некоторого времени. Однако заполнение пустот почти не влияет на окружающую структуру. [11]
Как мы увидим IB дальнейшем, в жидкой воде сохраняются фрагменты кристаллической структуры льда, и это объясняет многие ее свойства. [12]
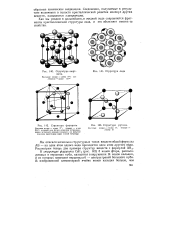 |
Структура вюрт.| Структура флуорита.| Структура рутила. [13] |
Как мы увидим в дальнейшем, в жидкой воде сохраняются фрагменты кристаллической структуры льда, и это объясняет многие ее свойства. [14]
Страницы: 1 2 3 4
