Кристаллическая структура - льд
Cтраница 3
Нейтральные молекулы могут образовывать раствор, не нарушая заметно тетраэдрического каркаса льда. Такие частицы внедряются в пустоты кристаллической структуры льда, а молекулы воды вокруг захваченной частицы становятся более упорядоченными, замороженными. Образуется нечто вроде айсбергов, которые в некоторых случаях при замораживании могут быть даже выделены в свободном состоянии в качестве индивидуальных кристаллических соединений - клатра-тов. Электролитическая диссоциация изменяет и фактическую концентрацию вещества. Так, при растворении в воде хлористый натрий полностью диссоциирует на ионы Na и С1 -, число частиц растворенного вещества при этом удваивается и концентрация возрастает вдвое. Согласно законам Рауля 7 ДГцип, АГПЛ и понижение давления пара растворителя пропорциональны молярной доле растворенного вещества, поэтому эффект электролитической диссоциации должен вдвое увеличить эти характеристики Если же электролитическая диссоциация веществ идет не до конца, а до состояния равновесия, то фактическая концентрация будет больше исходной. [31]
 |
Структура флуорнта.| Структура рутила. [32] |
На рис. 1.87 черные кружки показывают положение водорода, а штриховка - область, где сосредоточен отрицательный заряд. Как видно из рис. 1.87, кристаллическая структура льда имеет полости, что обусловливает его низкую плотность, меньшую плотности воды. Полости в кристаллической решетке льда могут заполняться другими молекулами, например СЩ, HzS, одноатомными молекулами благородных газов, в результате чего образуются своеобразные химические соединения. Соединения, получаемые в результате включения в полости кристаллической решетки молекул других соединений, называют клатратами. [33]
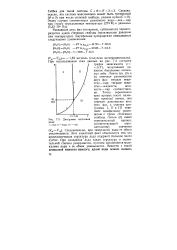 |
Диаграмма состояния воды. У-лед. / / - вода. III -пар. [34] |
Уж-УТВ) - Следовательно, при замерзании воды ее объем увеличивается. Этот известный факт объясняется тем, что кристаллическая структура льда содержит большое число пустот. При плавлении льда такая структура в значительной степени разрушается, пустоты заполняются молекулами воды и ее объем уменьшается. [35]
Эти гидраты принадлежат к типу клатратов ( см. разд. Образованию клатратов с водой благоприятствует наличие в кристаллической структуре льда многочисленных полостей. [36]
Известно, что для того, чтобы превратить в воду 1 г льда, находящегося при О С, необходимо затратить около 80 калорий теплоты. Эта теплота называется удельной теплотой плавления и расходуется на разрушение кристаллической структуры льда. [37]
Вода кипит под атмосферным давлением при 100 С, однако температура кипения воды аномальна вследствие наличия молекулярных ассоциаций; если бы их не существовало, то точка кипения воды была бы примерно равна 63 5 С. Жидкую воду всегда считают идеальным типом текучего тела и в то же время это жидкость, еще сохранившая воспоминания о кристаллической структуре льда, из которого она произошла ( К. [38]
Хотя водородные связи слабее ковалентных и ионных, они значительно прочнее вандерваальсовых связей и обусловливают ассоциацию молекул воды в жидком состоянии и некоторые аномальные свойства воды, в частности высокие температуры плавления и парообразования, высокую диэлектрическую проницаемость, максимальную плотность при 4 С, а также особую структуру льда. В кристаллах льда молекула воды образует четыре водородные связи с соседними молекулами воды ( за счет двух неподеленных электронных пар у кислорода и двух протонов), что обусловливает возникновение тетраэд-рической кристаллической структуры льда. [39]
Хотя водородные связи слабее ковалентных и ионных, они значительно прочнее вандерваальсовых связей и обусловливают ассоциацию молекул воды в жидком состоянии и некоторые аномальные свойства воды, в частности высокие температуры плавления и парообразования, высокую диэлектрическую проницаемость, максимальную плотность при 4 С, а также особую структуру льда. В кристаллах льда молекула воды образует четыре водородные связи с соседними молекулами воды ( за счет двух неподеленных электронных пар у кислорода и двух протонов), что обусловливает возникновение тетраэдрической кристаллической структуры льда. При высоких давлениях ( выше 200 МПа) обеспечивается более плотная укладка молекул воды и возникает еще несколько кристаллических модификаций льда. При плавлении происходит частичное разрушение структуры льда и сближение молекул, поэтому плотность воды возрастает. В то же время повышение температуры усиливает движение молекул, которое снижает плотность вещества. При температуре выше 4 С последний эффект начинает превалировать и плотность воды понижается. [40]
Еще совсем недавно предполагалось, что инертные элементы не обладают свойством вступать в химические реакции и образовывать истинные соединения. Были известны только их гексагидраты ( Кг - 6Н2О, Хе - 6Н2О), т.е. соединения включения ( клатраты), получающиеся в результате внедрения атомов криптона и ксенона в полости кристаллической структуры льда. [41]
На рис. 6.2 показаны области, соответствующие трем различньш кристаллическим модификациям льда. Всего их известно для Н2О шесть - три остальные могут существовать только при давлениях выше 2 - Ю8 Па. Перестройка кристаллической структуры льда при высоких давлениях ( переход лед I - лед II) приводит в точке В к изменению наклона кривой плавления ОБЕ. Это свидетельствует о том, что образование льда II из жидкой воды сопровождается уже не увеличением, а уменьшением объема, которое характерно для большинства веществ при всех давлениях. [42]
На рис. 6.2 показаны области, соответствующие трем различным кристаллическим модификациям льда. Всего их известно для Н2О шесть - три остальные могут существовать только при давлениях выше 2 - Ю8 Па. Перестройка кристаллической структуры льда при высоких давлениях ( переход лед I - лед II) приводит в точке В к изменению наклона кривой плавления ОБЕ. Это свидетельствует о том, что образование льда II из жидкой воды сопровождается уже не увеличением, а уменьшением объема, которое характерно для большинства веществ при всех давлениях. [43]
При 0 лед имеет гексагональную структуру. При температурах ниже - 80 удается получить кубическую структуру типа алмаза. Существу ют и другие кристаллические структуры льда, устойчивые при высоких давлениях. [44]
В твердой фазе вода также обладает аномальными свойствами. Поражает огромное разнообразие форм ледяных кристаллов ( снежинок) в атмосфере. В атмосферных условиях существует только одна из возможных кристаллических структур льда - гексагональная, тогда как при температурах ниже - 70 С кристаллы льда приобретают кубическую структуру, при еще более низких температурах лед вообще теряет свою кристаллическую структуру - он становится аморфным. [45]
Страницы: 1 2 3 4