Димерная структура
Cтраница 1
Димерная структура сохраняется во всех агрегатных состояниях кислот. Только воздействие высоких температур ( например, свыше 250 С для уксусной кислоты) может привести к распаду ассо-циатов на отдельные молекулы. [1]
Димерные структуры представляют собой переходный случай от молекул к координационным кристаллам, ибо у них уже число ближайших ( одновалентных) соседей превышает валентность центрального атома. Развитие полимеризации в двух или трех координатных направлениях приводит к образованию слоистого или пространственного каркаса, т.е. к кристаллической решетке. [2]
 |
Молекулы пентагалогенидов М2С1ю ( а и M4F2o ( о. [3] |
Димерные структуры реализуются у хлоридов, бромидов и у двух иодидов, тогда как тетрамеры и цепочки встречаются у фторидов. Как и в случае других галогенидов, молекулы типа М2С1ю ( рис. 9.12, а) или Д 4р2о ( рис. 9.12 6) могут укладываться различным образом, приводя к различным типам плотиейших упаковок атомов галогенов. В первом случае кубическая плотнейшая упаковка искаженная и симметрия является моноклинной. Это несколько напоминает рассмотренные ранее структуры трифтори-дов. [4]
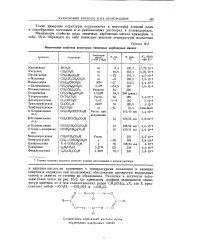 |
Физические свойства некоторых типичных карбоновых кислот. [5] |
Такие димерные структуры сохраняются в некоторой степени даже в газообразном состоянии и в разбавленных растворах в углеводородах. [6]
Такие димерные структуры сохраняются в некоторой степени даже в парообразном состоянии и в разбавленных растворах в неполярных растворителях. [7]
Такие димерные структуры образуют галогениды В, Al, Ga и других поливалентных элементов. Атомы галогенов, связывающие два металла, носят название мостиковых, остальные-концевые. [8]
В отличие от димерной структуры пентахлоридов и пентаброми-дов структурная ячейка пентафторидов тетрамерна. Атомы металлов в ней расположены по углам квадрата и связаны мостиками из атомов фтора. [9]
Обнаружено, что димерную структуру имеют также третичные алкилы и третичные арилы алюминия, такие как триметил ( 14), триэтил и трифенил. Но так как в этих структурах связь носит электронно-дефицитный характер ( мости-ковый атом углерода образует более, чем четыре связи), ее обсуждение мы отложим до гл. [10]
Сказанное свидетельствует о димерной структуре соединений, содержащих в одном из компонентов сильный хромофор. Кислородный атом при С, несущий отрицательный заряд, не может участвовать в образовании межмолекулярной ковалентной связи с другой молекулой из-за резонансной стабилизации бетаиновой структуры. Эти вещества дают водно-щелочные растворы, окрашенные в коричневато-желтый цвет. Гидрофобные свойства соединений обусловлены тем, что кислородный атом, несущий отрицательный заряд, трудно доступен для атаки катионом щелочного металла. В водно-щелочных растворах соединения, по-видимому, находятся в карбиноламинной форме. [11]
По-видимому, пентахлориды сохраняют свою димерную структуру в растворителях, не образующих комплексов, и в значительной степени - в расплаве. Мурью и др. [81 ] показали, что спектры комбинационного рассеяния твердого NbCl5, твердого ТаС15, раствора NbCl5 в сероуглероде и жидкого ТаС15 подобны. [12]
Данные измерений молекулярного веса здесь также отвечают димерной структуре; плоская конфигурация четырехковалентного ( dsp2) золота делает возможным существование цис-транс-изомеров, а также несимметричной структуры XXI. Высокий дипольный момент пропильного аналога ( СзН7АиВг2) 2 согласуется именно с несимметричной структурой. При реакции двухбромистого этилзолота с этилендиамином получается два продукта: [ Auen2 ] Br3 и [ ( С2Н5) 2Аиеп ] Вг, что опять-таки указывает на - несимметричную структуру. [13]
Этот метод позволил установить, что в природном лигнине димерные структуры р-арилового эфира арилглицерина ( см. схему 12.39, б) состоят из примерно равных количеств эритро - и рео-стереоизомеров. [14]
Может быть получеа и сольват Т1С14 - РОС13, имеющий димерную структуру. Два окта-эдрически расположенных атома титана в ней связаны через мостик из двух атомов хлора. Известны три кристаллические модификации этого соединения. [15]
Страницы: 1 2 3 4