Третичная структура - белковая молекула
Cтраница 1
Третичная структура белковой молекулы представляет собой трехмерные образования между полипептидными цепями. Спирали винтовой структуры белковой молекулы определенным образом изогнуты и упакованы в относительно жесткие конфор-мации. Устойчивость конформации третичной, а также четвертичной структуры обусловлена большим числом водородных, дисульфидных, ван-дер-ваальсовых и ионных связей. [1]
Что называется третичной структурой белковых молекул и за счет каких связей она поддерживается. [2]
Основной причиной инактивации ферментов является изменение третичной структуры белковых молекул. Упаривание ферментных растворов под вакуумом ( при t37 C) способствует сохранению ферментативной активности. Применение при упаривании пеногасителей основано на их способности вытеснять пенообразователь из поверхностного слоя и разрушать тем самым структуру пены. [3]
Сопоставление вторичных связей, принимающих участие в создании и сохранении третичной структуры белковой молекулы, показывает, что главную роль здесь играет не пептидный скелет, а боковые цепи аминокислот. Так как разные белки содержат в различных участках полипептидных цепей различные боковые цепи, то их взаимодействие приводит к своеобразной и строго определенной для каждого белка пространственной упаковке самих цепей. Какое-либо единообразие здесь невозможно, и потому белки сильно отличаются друг от друга именно по своей третичной структуре. [4]
 |
Схема молекулы миоглобина, составленная из проволочных моделей отдельных аминокислотных остатков. [5] |
Уже давно высказывалась гипотеза, что Организующим фактором в образовании третичной структуры белковой молекулы может служить тенденция к собиранию неполярных ( гидрофобных) остатков внутри белковой глобулы, а полярных ( гидрофильных) - на ее поверхности. Такая закономерность действительно проявилась в ммоглобине и гемоглобине. Молекулы воды, присоединенные к полярным радикалам, образуют вокруг глобулы двойной электростатический слой, что экранирует поле этих радикалов и уменьшает свободную энергию. При контакте гидрофобных радикалов с молекулами воды последние упорядочиваются, в результате чего уменьшается энтропия. Поэтому гидрофобным радикалам выгодно собраться внутри белковой молекулы и избежать контакта с молекулами воды. В то же время ван-дер-ваальсовое взаимодействие неполярных радикалов достаточно для объяснения притяжения и компактной укладки цепей внутри глобулы. [6]
Поверхностная активность белков, как и многие их функции, зависит от так называемой третичной структуры белковых молекул, которая обусловливается пространственной укладкой их полипептидных цепей. Эта третичная структура молекулы, в свою очередь, зависит от первичной структуры-последовательности аминокислот в молекуле, которая определяется генетическим аппаратом клетки. Поверхность белковой глобулы имеет мозаичный характер-содержит полярные и неполярные участки; при этом доля тех и других примерно одинакова, что характерно для всех белков, в том числе и мембранных. [7]
Подобные модификации структуры полипептида начинаются или сразу после трансляции, или еще до окончания формирования третичной структуры белковой молекулы. [8]
В случае белков необходимая структурная организация в области активного центра и отстоящих от него областях возникает в рамках третичной структуры белковой молекулы. Она определяется закодированным аминокислотным составом и последовательностью аминокислот в цепи и, следовательно, автоматически оказывается идентичной для всех белковых глобул. Но как добиться того же самого, хотя бы и не на столь сложном уровне, при создании полимерных катализаторов небелковой природы и можно ли вообще этого добиться, не повторяя всего безнадежно долгого для практики пути, которЬш прошла природа в процессе эволюции. [9]
В результате теплового или другого воздействия происходит также разрушение цистиновых связей белка, но основным фактором инактивации является изменение третичной структуры белковой молекулы. [10]
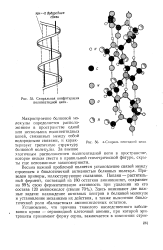 |
Спиральная конфигурация полипептидной цепи. [11] |
Макростроение белковой молекулы определяется расположением в пространстве одной или нескольких полипептидных цепей, связанных между собой водородными связями, и характеризует третичную структуру белковой молекулы. [12]
Макростроение белковой молекулы определяется расположением в пространстве одной или нескольких полипептидных цепей, связанных между собой водородными связями, и характеризует третичную структуру белковой молекулы. За внешне хаотичным расположением полипептидной цепи в пространстве, которое нельзя свести к правильной геометрической фигуре, скрыты еще непознанные закономерности. [13]
Кроме активных групп ( ферменты - протеиды) или активных центров ( ферменты - протеины) биокатализаторы имеют субстратный центр - участок ответственный за присоединение субстрата к ферменту и аллостерический центр, при присоединении к которому изменяется третичная структура белковой молекулы. Это присоединение приводит к изменению конфигурации активного центра и, как следствие, к увеличению или уменьше - - нию каталитической активности фермента. [14]
Если сравнить число этих исследований с прямыми рентгеноструктурными анализами в период за 1955 - 1960 гг., то мы увидим, что количество первых во много раз превосходит количество вторых. Но этими методами без применения рентгено-структурного анализа невозможно было решить вопросы третичной структуры белковых молекул. [15]
Страницы: 1 2