Металлическая структура
Cтраница 1
Металлические структуры обладают некоторыми очень характерными свойствами. Каждый атом в кристаллической структуре металла имеет высокое координационное число ( часто двенадцать и иногда восемь), и структура характеризуется высокой электро - и теплопроводностями. Атомы в металле располагаются близко один к другому; это означает, что наблюдается значительное перекрывание орбиталей внешних электронов и что валентные электроны фактически связаны не с отдельным ядром, а делокализованьг по всем атомам металла. Таким образом, металл можно рассматривать как ансамбль положительных ионов, которые, вообще говоря, представляют собой сферы одинакового радиуса ( марганец и уран являются исключениями), как можно более плотно упакованные в пространстве. Существует два способа плотной упаковки одинаковых сфер: один из них приводит к гексагональной, а другой - к кубической симметрии, но в каждом случае координационное число равно двенадцати. Объемноцентрированная кубическая структура щелочных металлов менее плотно упакована: для нее координационное число равно восьми и каждый ион имеет восемь ближайших соседей в услах окружающего его куба. [1]
 |
Упаковка ионов в кристалле NaCl.| Схема строения кристалла NaCl. [2] |
Металлическая структура, характерная для металлов в их твердом ( и жидком) агрегатном состоянии, является наиболее сложной. Эта структура содержит одновременно атомы нейтральные и ионизированные. В металлической структуре непрерывно осуществляется обмен электронами между нейтральными и ионизированными атомами без затраты энергии. [3]
Металлическая структура характеризуется относительно малой связью внешних валентных электронов в атомах металлов с ядром. Связь в решетке металла возникает в результате взаимодействия положительных ионов с электронным газом. Электроны, находясь между ионами, стараются стянуть их, стремясь уравновесить силы отталкивания, действующими между положительно заряженными ионами. [4]
Вследствие стабильной металлической структуры аустенит-ные стали сохраняют в течение длительного времени приемлемо низкую ползучесть даже при температурах выше 500 С. [5]
В металлических структурах атомные радиусы играют не менее важную роль, чем ионные в неорганических соединениях. [6]
 |
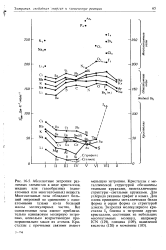
Микротвердрсть переходных металлов. [7] |
Процесс образования металлических структур из свободных атомов обычно рассматривают как результат взаимодействия газа из почти свободных валентных электронов с атомными остовами. Электронный газ стягивает положительно заряженные атомные остовы в ту или иную структуру. Образование предельно вырожденного электронного газа путем отрыва валентных электронов от свободных атомов требует больших энергий, равных сумме потенциалов ионизации. Энергии ионизации электронов возрастают от 4 - 5 эВ для щелочных металлов до 200 - 270 эВ для хрома, молибдена, вольфрама. В связи с этим необходим энергетический анализ и сопоставление теплот испарения, плавления и превращения металлов с энергией образования электронного газа. [8]
Последняя из типичных металлических структур - ОЦК ( калий, натрий, литий, ванадий... [9]
Силициды с металлическими структурами образованы замещением металлических атомов атомами кремния без перестройки решетки металла ( иногда с уплотнением), при котором наряду с металлическими связями между атомами имеются ковалентные. [10]
Кристаллы с металлической структурой обозначены темными кружками, неметаллические структуры-светлыми кружками. Для углерода указаны графит и алмаз. Для олова приведены металлическая белая форма и серая форма со структурой алмаза. [12]
 |
Изменения постоянных кристаллической структуры, вызванные вакансией ( о и атомом в междуузлиях ( б. [13] |
Вакансии в металлических структурах вызывают сжатие, а в ионных - расширение структур. [14]
Даже в изотропных металлических структурах узлов самолетов редко возникают однородные поля механических напряжений. В композиционных материалах за счет анизотропности структуры материала поля напряжений всегда анизотропны. Адгезионные соединения, таким образом, находятся в области несимметричных напряжений. Напряжения в адгезионных соединениях возникают уже во время процесса отверждения связующего при повышенной температуре. При определении геометрии соединения композитов адгезионным методом необходимо учитывать максимальные колебания напряжений, скорость изменения напряжения, необходимую размеростабильность соединения. [15]
Страницы: 1 2 3 4