Структурирование - вода
Cтраница 2
Величина статической ДП адсорбированной на аэросиле воды в пределах заполнения до 2 5 БЭТ-монослоев остается приблизительно постоянной, в то время как при адсорбции воды на пористом силикагеле она существенно уменьшается начиная с субмонослой-ных покрытий, что, вероятно, связано со структурированием воды в порах силикагеля. [16]
Однако свойства воды в таком физически сорбированном слое вследствие действия поверхностных сил отличаются от свойств объемной воды. Структурирование воды в тонких стенках, по-видимому, влияет на концентрацию и подвижность гидратирован-ных ионов, образующихся по реакции Н2О: Н адс ОН-адс - Учитывая, кроме того, чрезвычайно малый объем физически адсорбированной воды ( - 1016 молекул / см2), нет оснований ожидать заметных скоростей реакций с участием гидратированных ионов. Эта величина еще меньше в области отрицательных температур, где ионное произведение воды ( льда) быстро уменьшается. [17]
В данном случае в структурировании воды участвуют не только ионы Мд2, но и SO2 которые имеют более высокую энергию гидратации, чем ионы СГ. [18]
Является ли разделение гидрофильной и липофильной частей необходимым условием гомоионной ассоциации. Движущая сила ассоциации, вызванной структурированием воды, - минимизация нарушений структуры воды - прикладывается к любой паре больших ионов ( разд. Эту движущую силу увеличивают гидрофобные связи ( гл. [19]
Дрост-Хансен [27] суммировал доказательства существования подобного явления. Однако нет убедительного подтверждения, что такое упорядоченное структурирование воды может быть индуцировано поверхностью аморфного кремнезема, на которой SiOH-группы не имеют регулярного расположения на расстояниях, превышающих размеры между двумя или тремя силанольными центрами. [20]
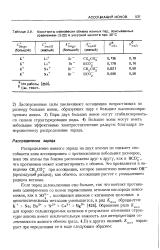 |
Константы оавновесия обмена ионных пар, описываемых уравнением в уксусной кислоте при 30 С. [21] |
Дисперсионные силы увеличивают ассоциацию возрастающих по размеру больших ионов, образующих пару с большим высокополяризуемым ионом. Пары двух больших ионов могут стабилизироваться силами структурирования воды. Большие ионы могут иметь небольшие эффективные электростатические радиусы благодаря поверхностному распределению заряда. [22]
Измерено [76] также рассеяние рентгеновских лучей насыщенными растворами фторида тетра-н-бутиламмония. Нередко считают, что ионы тетраалкиламмония способствуют структурированию воды. И действительно, РФР этих растворов удивительно походит на РФР воды при той же температуре. Нартен [76] попытался интерпретировать полученные РФР на основе двух моделей - газогидратной модели и своей собственной модели воды. В обеих моделях атомы фтора и азота, входящие в состав катионов, являются узлами решетки, связанной водородными связями, тогда как бутильные цепи катионов расположены в полостях решетки. Модель льда I в состоянии объяснить рентгеновские данные как для растворов, так и для воды, тогда как газогидратная модель, по-видимому, несовместима с РФР воды. Автор отмечает, что влияние катионов на структуру воды является двояким. Расстояние между ближайшими молекулами воды уменьшается с 2 85 А в чистой воде до 2 80 А в растворах, что указывает на некоторое упрочнение водородных связей. [23]
Описанный механизм, конечно, не является единственно возможным. Упоминаются и другие механизмы, приводящие к специфическому структурированию воды, содержащей ионы после ее магнитной обработки. [24]
По нашему мнению, эти результаты однозначно говорят в пользу сделанного ранее заключения о том, что структурный вклад в Д рС и ASpc доминирует над остальными, особенно в случае Ar-Rn. Таким образом, происходящее при растворении благородного газа структурирование воды оказывается выраженным тем сильнее, чем больше атомная масса благородного газа, радиус его атома, содержание дейтерия в воде и ниже температура. [25]
Прочность, жесткость и направленность водородных связей взаимозависимы друг от друга. Из-за направленности водородных связей их образование приводит к структурированию воды. Электростатические силы между молекулами воды способствуют оптимальной взаимной их ориентации, необходимой для образования водородных связей. Тепловое движение и действие дисперсионных сил мешает образованию водородных связей и ослабляет их. Образование водородной связи начинается с электростатического взаимодействия. Электростатическая связь при приближении молекул возникает мгновенно и не требует при этом от них жесткой взаимной ориентации. [26]
Действительно, как показали слектры ЯМР, в водных растворах вблизи молекул углеводородов период релаксации молекул воды в два раза больше, чем в воде, не содержащей растворенных углеводородов. Растворение углеводорода в воде приводит к равномерному распределению его молекул и, следовательно, к росту энтропии, однако из-за низкой растворимости углеводородов это увеличение энтропии не может компенсировать понижение энтропии системы, обусловленное структурированием воды в таком растворе. Уменьшение энтропии компенсирует процесс, ведущий к уменьшению границы контактов углеводородных цепей с водой, - ассоциацию углеводородных радикалов молекул ПАВ. В результате такой ассоциации уменьшается доля жидкости с повышенной структурированностью, и абсолютная величина понижения энтропии в растворе углеводородов или ПАВ становится равной абсолютной величине прироста энтропии, вызванного растворением углеводородов. Если в воде растворен углеводород, это явление ограничивает его растворимость и приводит к появлению углеводородной макрофазы ( жидкости) на границе с насыщенным водным раствором. Если же в растворе находятся дифильные молекулы ПАВ, ассоциация углеводородных радикалов не приводит к образованию макрофазы, так как этому препятствует гидратация полярных групп молекул или электростатическое отталкивание их ионов. В растворе ПАВ уменьшение энтропии, вызванное усилением структур жидкой воды, компенсируется увеличением степени ассоциации ПАВ и обусловливает появление критической концентрации ми-целлообразования. [27]
Представления о механизме возникновения гидрофобных взаимодействий, развиваемые Шерагой, подтверждаются при наблюдении ряда свойств водных растворов глобулярных белков и ПАВ. Исследование указанных систем представляется чрезвычайно плодотворным для получения экспериментальных доказательств основных предпосылок теории гидрофобного взаимодействия. Безусловно, необходимы и прямые исследования структурирования воды вблизи углеводородных молекул. Некоторые попытки таких исследований были выполнены Песиком и Клиффордом [71] с помощью ЯМР-спектроскопии, однако пока не получено ясных результатов. Тем не менее Герцем и Цайдлером [72] показано, что время релаксации молекул воды вблизи углеводородных молекул в 2 раза больше, чем у чистой воды. Создание количественной теории жидкой воды и, следовательно, детального механизма гидрофобных взаимодействий возможно только при комплексном рассмотрении данных, получаемых при исследованиях водных растворов как методом ЯМР, так и в результате разнообразных физико-химических исследований систем, свойства которых определяются гидрофобными взаимодействиями. [28]
Силы структурирования растворителя вначале были постулированы Диамондом [144] для объяснения наблюдаемого снижения коэффициента активности и осмотических коэффициентов водных органических солей при увеличении размера иона ( см. гл. Утверждается, что большая энергия образования полости в растворителях с высокой когезией, подобных воде, достигает минимального значения в растворах солей, состоящих из двух гидрофобно гидратиро-ванных ионов или одного гидрофобно, а другого отрицательно гидра-тированных ионов, если одна полость одновременно занята двумя ионами. Это называется ионной ассоциацией, усиленной структурированием воды. [29]
Проанализируем влияние электролита, присутствующего в растворе, на рассмотренные выше явления. Электростатическое поле иона нарушает, как бы плавит, водную решетку, поэтому структурирование воды под влиянием поверхностных полей не аналогично влиянию полей находящихся в растворе ионов. Самойлов ввел понятие о положительной и отрицательной гидратации. В зависимости от свойств ионы могут упорядочивать и разупорядочивать структуру объемной воды. Следовательно, до момента, когда контакт между частицами еще не стал кристаллизационным ( в результате выкристаллизовывания растворимого гидрата), свойства контакта могут как улучшаться, так и ухудшаться под влиянием растворенных ионов. Это справедливо для случая избытка раствора и не очень больших концентраций электролитов в растворе. [30]
Страницы: 1 2 3