Амаг
Cтраница 1
Закон Амага [ равенство (16.12) ] находит практическое применение при объемном анализе смесей идеальных газов. [1]
Ход кривой Амага для реального газа можно объяснить и другим способом, а именно как зависимость сжимаемости реального газа от давления. [2]
По закону Амага общий объем V смеси газов, химически не взаимодействующих друг с другом, равен сумме тех индивидуальных объемов Vi, которые занимал бы каждый из этих газов, взятый при той же температуре и под тем же давлением, что и газовая смесь. [3]
В опытах Амага, однако, установка была достаточно большой, для того чтобы две сферы из различных материалов могли быть помещены одна рядом с другой и, таким образом, могли быть проведены тонкие сравнительные измерения. Две сферы, участвующие в этих экспериментах, были изготовлены из резины и из бронзы. [4]
Эмиля Илэр Амага вспоминают в первую очередь, в связи с его исследованиями сжимаемости газов и жидкостей в области давлений до 3000 кгс / см2 и температур до 200 С. [5]
Аналогично закону Дальтона Амага предложил закон аддитивности парциальных объемов, согласно которому общий объем газовой смеси равен сумме парциальных объемов ее компонентов. [6]
В первом опыте Амага заметил, что очень малая величина внешнего давления увеличивает на 300 делений уровень воды в капиллярной трубке, присоединенной к резиновой сфере, в то время как в капиллярной трубке, присоединенной к бронзовой сфере, та же самая величина давления даже почти не вызывает движения мениска. [7]
Минимум на изотерме Амага соответствует той плотности, когда оба эффекта ( влияние собственного объема молекул и влияние межмолекулярного сцепления) уравновешивают друг друга. [8]
Поскольку ход изотерм Амага вверх объясняется перевесом межмолекулярных сил отталкивания над силами притяжения, то можно заключить, что даже в сильно разреженном газе ( р - - 0) при температурах выше температуры Бойля Тв перевес всегда на стороне сил отталкивания. [9]
Дальтона, закон Амага или правило аддитивности псевдоприве-деппых свойств газовой елеен. [10]
Равенство (2.176) выражает закон Амага. [11]
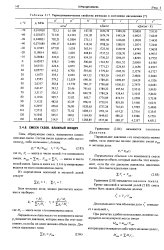 |
Термодинамические свойства аммиака в состоянии насыщения. [12] |
Уравнение (2.85) называется законом Амага. [13]
Для идеальных газов закон Амага непосредственно вытекает из их уравнения состояния. [14]
Это отношение иногда называют числом Амага, который занимался изучением сжимаемости газов. [15]
Страницы: 1 2 3 4