Амаг
Cтраница 3
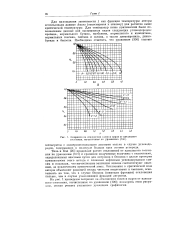 |
Поправки на отклонения газов и паров от идеального состояния, вычисленные по уравнению ( 100. [31] |
Для нахождения зависимости / как функции температуры авторы использовали данные Амага ( относящиеся к этилену) для расчетов выше критической температуры. Для температур ниже критической были использованы данные для насыщенных паров следующих углеводородов: пропана, нормального бутана, изобутана, нормального и изопентана, нормальных гексана, гептана и октана, а также диизопропила, диизо-бутила и бензола. [32]
Уравнение (11.108) называется уравнением Дальтона, а (11.111) - уравнением Амага, по имени ученых, впервые их устанозивших опытным путем. [33]
Темкина в случае умеренных заполнений, но не с изотермой Амага. Те же результаты получаются на основе анализа очень точных значений адсорбированных количеств, вычисленных Грэмом [6] из емкостных измерений, хотя такие значения сейчас имеются только для 0 1 N растворов. [34]
Уравнение (1.68) выражает закон Дальтона, а уравнение (1.69) - закон Амага. [35]
Заметим, что vt при этом описывается в соответствии с приближенным законом Амага, а ф - в соответ-стви с приближенным правилом Льюиса. [36]
В конце прошлого и начале этого века вопрос о сжимаемости жидкостей исследовал французский ученый Амага, доводивший давления, производимые на жидкости, до 3000 атм, а в последнее время ( сороковые годы этого столетия) американский ученый Бриджмен достигал давлений 150 000 атм. [37]
В этих таблицах значения плотности d и степени сжимаемости pV выражены в единицах амага. [38]
Если смесь идеальна ( см. раздел VI.20), то для нее справедлив закон Амага, который гласит, что объемы чистых компонентов аддитивны при постоянных давлении и температуре. [39]
Существует несколько способов определения коэффициента сжимаемости г, из которых наиболее известны метод псевдокритических параметров и метод Амага. [40]
На рис. 1 - 16 показано совмещение сеток с изотермами для углекислоты, воздуха и эфира по методу Амага. Приводя сетки изотерм для указанных газов в соответствующие системы координат, Амага блестяще подтвердил выводы Ван-дер - Ваальса о том, что в соответственных состояниях газы в отношении давления, объема и температуры становятся идентичными. [41]
Уравнение ( 8 - 29) означает, что в общем случае для такой смеси несправедлив и закон Амага. [42]
Другим широко используемым путем представления р - V - Г - свойств газовых смесей является закон аддитивности индивидуальных объемов Амага. [43]
В некоторых случаях, даже когда компоненты, составляющие смесь, являются неидеальными газами, смесь в целом достаточно хорошо подчиняется закону Амага. [44]
Здесь PQ и vn давление и удельный объем воздуха при нормальных физических условиях, а отношение pv / pava - так называемое число Амага. [45]
Страницы: 1 2 3 4