Парная аддитивность
Cтраница 2
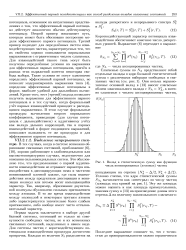 |
Вклад в статистическую сумму как функция числа ионизированных ( атомных частиц. [16] |
В тех случаях, когда в системе возможно образование связанных состояний, приближение ( 6), ( 10), хорошо работающее в слабонеидеальном или высокотемпературном случаях, недостаточно для описания сильнонеидеальных систем. Это обусловлено тем, что предположение о парной аддитивности взаимодействия не отражает характера взаимодействия в диссоциирующих газах и частично ионизованной плотной плазме, где силы взаимодействия между продуктами диссоциации и ионизации молекул или атомов носят насыщающийся характер. Так, например, образование двухатомной молекулы обусловлено сильным притяжением между атомами. В то же время взаимодействие между молекулой и некоторым третьим атомом либо характеризуется значительно более слабым притяжением, либо вообще имеет чисто отталки-вательный характер. [17]
Установленная аналогия позволяет использовать для нахождения избыточных термодинамических величин раствора метод ви-риальных разложений, изложенный в главе IV. Кроме того, еще требуется предположение о парной аддитивности потенциала средней силы. В пределе бесконечно разбавленного раствора газ растворенного вещества становится идеальным. [18]
Разумеется, фактическое нахождение средних плотностей сохраняющихся величин и потоков предполагает известной функцию распределения. Поскольку все эти плотности имеют од-ночастичный и двухчастичный характер ( благодаря парной аддитивности энергии взаимодействия), то достаточно знать одно-частичную и двухчастичную функции. [19]
Первоначальное исследование лондоновских взаимодействий между молекулами было в основном связано с проблемой межмолекулярных сил в газах, где среднее расстояние между молекулами сравнимо с длиной волны основных взаимодействий. В этом случае притяжение существенно только между несколькими соседними молекулами и поэтому предположение о парной аддитивности притяжения оказывается вполне оправданным. То же приближение допускается и Гамакером, поскольку при вычислении притяжения между конденсированными телами суммирование по взаимодействующим, принадлежащим различным частицам элементам объема, производится так, как если бы эти элементы были полностью изолированными. Однако это допущение неправомерно. Действительно, практически каждый элемент объема частицы окружен многими другими элементами, образующими в совокупности саму частицу и сильно взаимодействующими между собой. [20]
Так, молекула газа может притягивать все соседние молекулы одновременно, а не только ту молекулу, которая окажется в непосредственной близости в данный момент времени. Эта черта лондоновского взаимодействия существенно отличает его от кеезомовских и дебаевских полей и является основой концепции парной аддитивности лондоновского притяжения. [21]
В заключение целесообразно привести некоторые замечания. На первый взгляд кажется, что то же самое имеет место и при рассмотрении многочастичных комплексов в приближении парной аддитивности потенциальной энергии. Однако, использующееся при этом предположение о парной аддитивности потенциальной энергии само по себе уже является приближением в случае рассмотрения многочастичных комплексов. Это приближение может быть достаточно хорошим лишь в случае центральных сил, действующих между исходными атомами. Иначе говоря, это приближение может считаться оправданным при описании взаимодействия атомов в основном состоянии, когда полный момент импульса, а следовательно и магнитный момент атома равен нулю, а также при рассмотрении образования молекул в основном состоянии. В этом случае приближение о парной аддитивности потенциальной энергии может оказаться достаточно грубым. Особенно ярко это проявляется при описании взаимодействия частиц в полярных жидкостях и газах, состоящих из полярных молекул. В этом случае, как показано, например в [177], вклад неаддитивных добавок в старшие вириальные коэффициенты, связанный с наличием собственного дипольного момента молекул, оказывается того же порядка величины, что и соответствующая аддитивная часть вириального коэффициента. [22]
В-третьих, как следует из вышеизложенного, для получения информации по межмолекулярным силам необходимо использовать В ( Т) вместе с другими данными. Наилучшими для этих целей являются данные по коэффициентам переноса и сечению рассеяния молекулярных пучков, так как они зависят только от двойного взаимодействия и при этом ле ставится вопрос о парной аддитивности. Данные по С ( Т) и свойствам кристалла менее удовлетворительны. Если имеются только данные по В ( Т) и С ( Т), то бесполезно пытаться строить очень сложную модель, так как она не будет иметь большого физического смысла. [23]
Это являемся, по-видимому, следствием сравнительно малой длины изученных цепей ( 10 шагов), небольшого среднего числа частиц в основном образце ( - - 30), использованных приближении при подсчете энергии, предположения о парной аддитивности энергии взаимодействия частиц. [24]
Ряд особенностей присущ тройным смесям полимеров, которые находят все более широкое практическое применение. Большинство свойств тройных систем с изменением состава меняются без экстремумов, монотонно. Принцип парной аддитивности [67] позволяет с достаточной точностью оценивать свойства тройных систем, исходя из свойств бинарных смесей определенного состава. Известно, что структура и свойства бинарных смесей в значительной мере определяются интенсивностью взаимодействий между компонентами. В тройной смеси кроме бинарных существуют и тройные взаимодействия полимеров. Принцип парной аддитивности сформулирован в предположении, что тройные взаимодействия ( с учетом трехфазности системы) несущественны и изменение свойств происходит по закону, близкому к аддитивности. На рис. 25 точка О в треугольнике составов отвечает некой тройной смеси, которая может быть получена смешением соответствующих количеств ( pi2, ф2з, Ф1з) бинарных смесей. [26]
В заключение целесообразно привести некоторые замечания. На первый взгляд кажется, что то же самое имеет место и при рассмотрении многочастичных комплексов в приближении парной аддитивности потенциальной энергии. Однако, использующееся при этом предположение о парной аддитивности потенциальной энергии само по себе уже является приближением в случае рассмотрения многочастичных комплексов. Это приближение может быть достаточно хорошим лишь в случае центральных сил, действующих между исходными атомами. Иначе говоря, это приближение может считаться оправданным при описании взаимодействия атомов в основном состоянии, когда полный момент импульса, а следовательно и магнитный момент атома равен нулю, а также при рассмотрении образования молекул в основном состоянии. В этом случае приближение о парной аддитивности потенциальной энергии может оказаться достаточно грубым. Особенно ярко это проявляется при описании взаимодействия частиц в полярных жидкостях и газах, состоящих из полярных молекул. В этом случае, как показано, например в [177], вклад неаддитивных добавок в старшие вириальные коэффициенты, связанный с наличием собственного дипольного момента молекул, оказывается того же порядка величины, что и соответствующая аддитивная часть вириального коэффициента. [27]
Во-первых, тот факт, что газы конденсируются в жидкости, позволяет сделать предположение о существовании сил притяжения между молекулами на больших расстояниях. Во-вторых, очень сильное сопротивление жидкостей сжатию свидетельствует о том, что на небольших расстояниях действуют силы отталкивания, резко изменяющиеся с расстоянием. При условии парной аддитивности сил можно ожидать, что потенциальная энергия взаимодействия между двумя молекулами изменяется таким образом, как показано на фиг. Эта потенциальная энергия может зависеть также от ориентации, если молекулы не являются сферически симметричными, а в некоторых случаях иметь отклонения ( на фиг. Квантовая механика дает обширную информацию о форме кривой потенциальной энергии, однако точные расчеты на основании этой информации не всегда возможны. Не рассматривая эту дополнительную информацию, поставим перед собой следующий вопрос: возможно ли в принципе однозначное определение межмолекулярной потенциальной энергии, если известна зависимость второго вири-ального коэффициента от температуры. [28]
Ряд особенностей присущ тройным смесям полимеров, которые находят все более широкое практическое применение. Большинство свойств тройных систем с изменением состава меняются без экстремумов, монотонно. Принцип парной аддитивности [67] позволяет с достаточной точностью оценивать свойства тройных систем, исходя из свойств бинарных смесей определенного состава. Известно, что структура и свойства бинарных смесей в значительной мере определяются интенсивностью взаимодействий между компонентами. В тройной смеси кроме бинарных существуют и тройные взаимодействия полимеров. Принцип парной аддитивности сформулирован в предположении, что тройные взаимодействия ( с учетом трехфазности системы) несущественны и изменение свойств происходит по закону, близкому к аддитивности. На рис. 25 точка О в треугольнике составов отвечает некой тройной смеси, которая может быть получена смешением соответствующих количеств ( pi2, ф2з, Ф1з) бинарных смесей. [29]
В заключение целесообразно привести некоторые замечания. На первый взгляд кажется, что то же самое имеет место и при рассмотрении многочастичных комплексов в приближении парной аддитивности потенциальной энергии. Однако, использующееся при этом предположение о парной аддитивности потенциальной энергии само по себе уже является приближением в случае рассмотрения многочастичных комплексов. Это приближение может быть достаточно хорошим лишь в случае центральных сил, действующих между исходными атомами. Иначе говоря, это приближение может считаться оправданным при описании взаимодействия атомов в основном состоянии, когда полный момент импульса, а следовательно и магнитный момент атома равен нулю, а также при рассмотрении образования молекул в основном состоянии. В этом случае приближение о парной аддитивности потенциальной энергии может оказаться достаточно грубым. Особенно ярко это проявляется при описании взаимодействия частиц в полярных жидкостях и газах, состоящих из полярных молекул. В этом случае, как показано, например в [177], вклад неаддитивных добавок в старшие вириальные коэффициенты, связанный с наличием собственного дипольного момента молекул, оказывается того же порядка величины, что и соответствующая аддитивная часть вириального коэффициента. [30]
Страницы: 1 2 3
