Субтилизина
Cтраница 1
 |
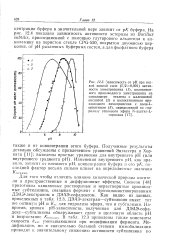
Эффективность аминоацилирования, осуществляемого нативной ( Thr-51 и модифицированной ( А1а - 51 и Рго-51 тирозил-т РНК-синтетазами1. [1] |
Субтилизины - сериновые протеиназы, секре-тируемые в культуральную среду грамположи-тельными бактериями, - широко используются в качестве биодеградируемых детергентов. Все они прочно связывают один или несколько атомов кальция, повышающих их стабильность. К сожалению, субтилизины используются в таких промышленных процессах, где участвуют в больших количествах соединения, хела-тирующие металлы, в том числе кальций, и в таких условиях субтилизины быстро теряют свою активность. [2]
Хотя полипептидные цепи а-химотрипсина и субтилизина свернуты совершенно различными способами, аминокислотные остатки, участвующие в катализе ( серии, гистидин и аспарагиновая кислота), располагаются в пространстве одинаково. [3]
Ричарде показал, что в определенных условиях субтилизин расщепляет в РНКазе пептидную саязь Ala-20 - Ser-21. Образующиеся фрагменты были названы S-пептидом ( остатки 1 - 20) и S-белком ( остатки 21 - 124); за счет нековалент-ных взаимодействий фрагменты образуют комплекс, названный РНКазой S. Этот комплекс обладает почти полной каталитической активностью нативного фермента; в изолированном виде S-пептид и S-белок неактивны. Далее было установлено, что синтетический пептид, идентичный по последовательности фрагменту S-пептида, содержащему остатки с 1 по 13, восстанавливает активность S-белка, однако более короткий пептид, содержащий остатки с 1 по II, такой способностью не обладает. Полученные данные позволили сделать заключение о том, что соответствующие остатки His-12 или Met-13 ( или оба этих остатка) входят в активный центр фермента. [4]
Свенсон [48] приготовил одинаковые растворимые и нерастворимые производные субтилизина, связывая фермент с бромцианактнвированным ДЭАЭ-декстраном и ДЭАЭ-сефадексом. Как видно из данных, приведенных в табл. 12.3, ДЭАЭ-декстран-субтилизин имеет тот же оптимум рН и Кт для гидролиза эфира, что и субтилизин. [6]
Таким образом, именно совершенствование каталитических поверхностей химотрипсина и субтилизина привело к принятию ими одинаковой функции. Как показано на рис. 11.1, механизм каталитического действия протеаз папаина и глицеральдегид-3 - фосфатдегид-рогеназы, фермента гликолитического пути, по-видимому, аналогичен механизму действия сериновых протеаз. [7]
Bacillus subtilis содержится особое бактериолитическое вещество, получившее название субтилизин. [8]
Связанные с белками соединения можно выделять и без гидролиза, с помощью специфических ферментов, например субтилизина. [9]
На основании данных, относя: щихся к миоглобину, лизоциму, папаину и а-химотрипсипу, была предсказана структура а - и р-цепей гемоглобина, рибонуклеа-зы А, субтилизина BPN и фрагмента карбоксипептидазы. Согласие с опытом было получено для 74 % аминокислот. [10]
Однако на примере ряда ферментов, и рибонуклеазы в частности, было показано, что не вся молекула, а лишь некоторая ее часть ( активный участок) ответственна за каталитическую активность. Так, Ричарде, используя фермент субтилизин, расщепил молекулу рибонуклеазы по связи между звеньями 20 н 21 ( пептидная связь Ala - Ser), и при этом вторичная и третичная структуры удержали молекулу как целое. [11]
Однако на примере ряда ферментов, и рибонуклеазы в частности, было показано, что не вся молекула, а лишь некоторая ее часть ( активный участок) ответственна за каталитическую активность. Так, Ричарде, используя фермент субтилизин, расщепил молекулу рибонуклеазы по связи между звеньями 20 и 21 ( пептидная связь Ala - Ser), и при этом вторичная и третичная структуры удержали молекулу как целое. [12]
С другой стороны, известны молекулы белков, которые резко отличаются друг от друга первичной, вторичной и третичной структурами, но несмотря на это, обладают сходной биологической активностью. Классическим примером могут служить химотрипсин и бактериальная протеиназа субтилизин. Несмотря на существенные различия в структурах, основные аминокислоты активных центров этих ферментов идентичны и осуществляют свои каталитические функции по сходному механизму. По-видимому, такие белки являются результатом пересечения путей эволюции. [13]
 |
Влияние рН на адсорбцию нейтральной протеазы на сефарозе 4В, замещенной триэтилентетрамином, янтарным ангидридом, триэтилентетрамином и хлорацетил - О-фенилала-нином Г401. [14] |
Нейтральная протеаза эффективно адсорбируется в интервале рН 5 - 6 5 и таким образом отделяется как от субтили-зина, так и от других белков, присутствующих в фильтрате культуры. При более высоких рН нейтральная протеаза не может быть эффективно отделена от субтилизина. Из комплекса с иммобилизованным аффинным лигандом нейтральную протеазу освобождают, повышая рН, до значений, при которых связывание субстрата уже ослабевает, но денатурация фермента еще не происходит. [15]
Страницы: 1 2