Сульфамида
Cтраница 1
N-замещенкые сульфамиды не реагируют с изоцианатами в исследованных до настоящего времени условиях. [1]
С сульфамидами, синтезированными из диариламинов [71], получены по существу аналогичные результаты: л-толуолсуль-фофенил-л - толиламид при обработке концентрированной серной кислотой дает 2 сульфона и сульфокислоту. [2]
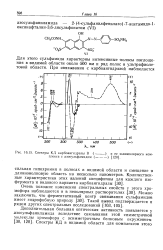 |
Спектры КД карбоангидразы В (. [3] |
Для этого сульфамида характерны интенсивные полосы поглощения в видимой области около 500 нм и ряд полос в ультрафиолетовой области. [4]
После охлаждения сульфамид отсасывают и очищают перекристаллизацией из воды или 50 % - ного спирта. [5]
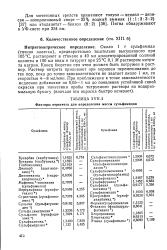 |
Факторы пересчета для определения массы сульфамидов. [6] |
Около 1 г сульфамида ( точная навеска), предварительно тщательно высушенного при 105 С, растворяют в стакане в 40 мл концентрированной соляной кислоты и 100 мл воды и титруют при 25 С 0 1 М раствором нитрита натрия. Конец бюретки при этом должен быть погружен в раствор. Раствор нитрита приливают при хорошем перемешивании до тех пор, пока до точки эквивалентности не хватает около 1 мл, со скоростью 4 - 8 мл / мин. [7]
Аминогруппа фталимида или сульфамида вследствие оттягивания электронов обеими карбонильными группами или сульфонильной группой не обладает достаточно основным характером для реакции с алкилгалогенидами. Напротив, она обладает кислотным характером, поэтому со щелочами образуются соли, которые и используют в реакции. [8]
В щелочных растворах сульфамиды, вероятно, вытесняются из координационной сферы конкурирующими гидроксильными ионами. [9]
В этом отношении сульфамиды и сульфанилиды ведут себя аналогично нафтолам. [10]
Получаемые из сульфохлоридов сульфамиды не менее чем с четырьмя алифатически связанными атомами углерода представляют собой воскообразные или маслоподобные вещества, широко используемые в качестве пластификаторов. Октадецилсульфохлорид и его гомологи реагируют также с морфолином при 0 - 4 С с образованием соответствующих 4 - ( алкилсульфо) - морфолинов, которые фирма Monsanto Chemical121 использует для переработки поливинилхлорида. Вследствие наличия гетероцикла и 802-грушгы в этих соединениях они являются активно растворяющими пластификаторами. [11]
Замещенные у азота сульфамиды могут быть получены из сульфохлоридов и первичных или вторичных оснований. Зачастую реакция протекает легче в присутствии пиридина. Так например образуется толуол-р-сульфондифениламид из р-толуолсульфохло-рида и дифениламина. При проведении реакции без пиридина необходимо нагревать до 150, причем в качестве побочных продуктов получаются синий краситель и смолистые вещества. [12]
В некоторых случаях сульфамиды расщепляются при нагревании с хлорсульфоновой кислотой. Это не гидролиз в точном смысле этого слова, однако этим способом амии может быть получен из продуктов реакции, Бензолсульфодиалкиламиды [546, 72] при нагревании с хлорсульфоновой кислотой при 130 - 150 в течение 2 - 3 час. [13]
В присутствии щелочи сульфамиды легко реагируют с хлоран-гидридами сульфокислот, давая дисульфимиды, которые часто мешают идентификации первичных аминов по реакции Гинзберга. [14]
В результате деструкции сульфамиды образуют характерные гетероциклические амины, на основе которых и проводят определение сульфамидных препаратов в биологических жидкостях. [15]
Страницы: 1 2 3 4