Сульфат - палладий
Cтраница 1
Сульфат палладия, PdS04 - 2H20, осаждается при упаривании на холоду раствора Pd ( OH) 2 в серной кислоте или металлического палладия в горячей конц. [1]
Сульфат палладия PdSO4 - 2H20 получается при нагревании палладия с концентрированной серной кислотой или при выпаривании азотнокислого раствора с серной кислотой. Безводная соль малорастворима в концентрированной серной кислоте, но хорошо растворяется в воде с образованием оранжевого или желтого раствора, из которого выпариванием могут быть получены красновато-коричневые расплывающиеся кристаллы. При кипячении сильнокислого раствора со спиртом или щавелевой кислотой осаждается металлический палладий. [2]
Сульфат палладия состава PdSO4 2Н2О образуется при растворении палладия в смеси серной и азотной кислот. Сульфат палладия устойчив лишь в кислых растворах, в воде легко гидролизуетея с образованием нерастворимых продуктов гидролиза - основных сульфатов типа PdSC4 7PdO 6Н2О или гидрата окиси палладия. Это указывает на значительную диссоциацию комплексного иона в водных растворах. [3]
Сульфат палладия состава PdSO4 - 2H2O образуется при растворении палладия в смеси серной и азотной кислот. Соединение подобного состава образуется при растворении гидрата окиси палладия в серной кислоте. Сульфат палладия устойчив лишь в кислых растворах, в воде легко гидролизуется с образованием нерастворимых продуктов гидролиза - основных сульфатов типа PdSO4 7PdO - 6H2O или гидрата окиси палладия. Это указывает на значительную диссоциацию комплексного иона в водных растворах. [4]
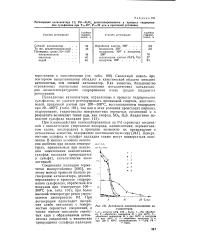 |
Активность алюмопалладиевых катализаторов. [5] |
Поверхностные сульфид и сульфат палладия также могут подвергаться окислению. В мягких условиях окисления особенно при низких температурах, применяемых при окислении химическими окислителями, сульфид палладия превращается в сульфат, каталитически мало активный. [6]
Бромид в водных растворах реагирует с сульфатом палладия с образованием соединений с характерным спектром поглощения в ультрафиолетовой области. Метод позволяет определять 0 5 - 7 0 мкг / мл бромида. [7]
Индикаторный порошок пропитан раствором молибдата аммония и сульфата палладия. При действии окиси углерода происходит каталитическое восстановление желтого силикомолибденового комплекса в синий цвет. [8]
Колориметрическое определение-с применением индикаторной трубки с силикагелем, пропитанным раствором сульфата палладия, основано на почернении индикаторного порошка. Шефер пропитывает силикагель раствором молибдата аммония и сульфата палладия. В зависимости от концентрации СО индикаторный порошок окрашивается от серо-зеленого до сине-зеленого цвета. Окраска сравнивается с искусственной шкалой. [9]
Колориметрическое определение с применением индикаторной трубки с силикагелем, пропитанным раствором сульфата палладия, основано на почернении индикаторного порошка. Шефер пропитывает силикагель раствором молибдата аммония и сульфата палладия. В зависимости от концентрации СО индикаторный порошок окрашивается от серо-зеленого до сине-зеленого цвета. Окраска сравнивается с искусственной шкалой. [10]
Колориметрическое определение с применением индикаторной трубки с силикагелем, пропитанным раствором сульфата палладия, основано на почернении индикаторного порошка. [11]
Смешивают 75 мл дистиллированной воды, 45 мл рас-гвора парамолибдата аммония и 10 мл раствора сульфата палладия. [12]
Смешивают 75 мл дистиллированной воды, 45 мл раствора парамолибдата аммония и 10 мл раствора сульфата палладия. [13]
Смешивают 75 мл дистиллированной воды, 45 мл раствора молнодата аммония и 10 мл раствора сульфата палладия. [14]
При протягивании воздуха, содержащего окись углерода, через индикаторную трубку с силикагелем, пропитанным раствором сульфата палладия, индикаторный порошок окрашивается в черный цвет. Интенсивность окраски измеряют по искусственной стандартной шкале. [15]
Страницы: 1 2 3