Сульфат - церие
Cтраница 3
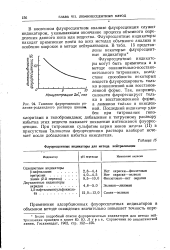 |
Гашение флуоресценции ро-дамин-роданидного раствора цинком.| Флуоресцентные индикаторы для метода нейтрализации. [31] |
При титровании сульфатом церия ионов железа ( II) в присутствии силоксена флуоресценция раствора наоборот исчезает после добавления избытка окислителя. [32]
С; растворимы сульфат церия, нитрат аммония-церия, сульфат аммония-церия, карбонаты и салицилаты церия. [33]
Сульфат церия ( сульфат церия и его гидраты, гидратированный сульфат церия, представляющий собой оранжево-желтые призмы, растворимые в воде) используется в фотографии как восстановитель. Имеются также и двойные сульфаты церия. [34]
Таким образом, сульфат церия ( 1У) полнее окисляет железо ( П), чем азотная кислота. [35]
Дозиметр на основе сульфата церия применяется в интервале энергий 0 1 - 2 Мэв при мощности дозы в пределах 2 - Ю3 - 2 8 - 108 эрг / ( г-ч) при полной дозе до 1012 эрг / кг. Так как разбавленные растворы чувствительны к фотовосстановлению, они должны храниться в темноте. Степень восстановления иона Се4 может определяться титрованием или колориметрически. [36]
Для изготовления растворов сульфата церия прокаливают осажденный щавелевокислый церий приблизительно при 600 до СеО2 и некоторое время обрабатывают при 125 - 130 серной кислотой ( уд. Наконец, отфильтровывают еще теплый раствор от непрореагировавшей окиси. [37]
Правильно приготовленные растворы сульфата церия являются для ультрамикроанализа, повидимому, наиболее пригодными. Перед приготовлением реактива воду и серную кислоту следует подвергнуть перегонке в стеклянном приборе со шлифами. При наличии такого прибора перегонка концентрированной серной кислоты не составляет большого труда. К колбе для перегонки емкостью приблизительно 50 - 100 мл присоединяют на шлифе стеклянный воздушный холодильник длиной 60 - 65 см. Серную кислоту помещают в колбу. Перед установлением правильного режима кипения кислота сначала бурлит и дымит, что связано с наличием в ней воды. После удаления воды кислота перегоняется значительно быстрее и спокойнее. [38]
Преимуществом использования растворов сульфата церия в кислой среде является то, что при этом не образуется промежуточных продуктов восстановления церия ( IV) и, следовательно, на любой термометрической кривой будет только одна эквивалентная точка. [39]
Кривая потенциометрического титрования сульфата церия ( IV) ( 2 мл) в среде H2S04 ( 1: 4) раствором сульфофенилазохромот-роповой кислоты представлена на рис. 5; титрант прибавляли порциями через 5 мин. [40]
Образовавшийся ферроцианид титруется сульфатом церия [1247] в кислом растворе с ферроином в качестве индикатора. [41]
Восстановленный Мо титруют сульфатом церия. [42]
Ванадат натрия [836], сульфат церия ( 1У) [594], перекись водорода, монохлориод [177] в кислой среде окисляют тиосульфат до тетратионата, хлор, бром, хлорамин Т [1123] и хлорамин, Б [1299] - до сульфата. [43]
 |
ПОТЕРЯ воды восьмиводными. [44] |
Несоответствие между значениями растворимости сульфата церия при указанных температурах заставляет предположить, что данные для 20 и 40 С, полученные в 1930 г., по-видимому, неверны. Расхождения между данными для других сульфатов не выходят за пределы ошибки опыта. [45]
Страницы: 1 2 3 4