Сульфид - хром
Cтраница 3
Моносульфиды металлов с / 4 ( Сги) и rf9 ( Cun) имеют особые, присущие только им структуры. Сульфид хрома будет описан несколько позже в этой главе. Структура CuS ( ковеллит) представляется совершенно необъяснимой, если считать, что это соединение Си11; в действительности же система Си-S чрезвычайно сложна; она обсуждается в гл. [31]
Кристаллохимические свойства сульфидов хрома рассмотрены в работах [ 338, с. Система Cr-S изучена при комнатной температуре. В препаратах с содержанием металла до Cr0) 88S равновесие достигается быстро, в препаратах с более высоким содержанием хрома равновесия достичь трудно. [32]
А) почти вдвое больше, чем у атомов кислорода ( 0 6 А), Механизм защитного действия легирующих элементов, в частности хрома, А. В. Смирнов усматривает в том, что эти эле менты, образуя твердый раствор с железом, уменьшают его взаимодействие с серой. Возможность образования защитных покровов на основе сульфидов хрома им отвергается. [33]
Гидролизуется ли сульфид марганца. Ответ поясните, сравнив сульфид марганца с сульфидом хрома. [34]
Если вещество подвергается необратимому гидролизу, то его синтез осуществляют в неводных средах или в условиях, исключающих присутствие растворителей. В частности, получение сульфида алюминия А128з или сульфида хрома ( III) Сг28з производят только методом непосредственного взаимодействия металлов с серой. [35]
Его защитное действие состоит в образовании во внутреннем слое пленки решетки насыщенного раствора сульфида хрома в FeS, обладающего малой концентрацией дырок. [36]
Хром, подобно марганцу, ослабляет отрицательную роль серы в образовании кристаллизационных трещин. Обладая более высоким, чем железо, химическим сродством к сере, хром связывает ее в тугоплавкий сульфид хрома. [37]
Хром, подобно марганцу, ослабляет отрицательную роль серь в образовании кристаллизационных трещин. Обладая более высо ким, чем железо, химическим сродством к сере, хром связывав ее в тугоплавкий сульфид хрома. [38]
Исходный Cr2S3 получали сульфидизацией сероводородом сульфата хрома при 500 С, так как для синтеза Cr2S5 нужен наиболее реакционно способный полуторный сульфид хрома. Полисульфид хрома неустойчив и разлагается на Cr2S3 и серу при нагревании до 120 С или длительном хранении на воздухе. [39]
 |
Сравнительные скорости окисления защищенных. [40] |
Хромирование несколько более устойчиво, но не всегда прочно и отстает от основного металла. Кроме того, серный ангидрид, обычно присутствующий в продуктах сгорания сернистых топлив, при некоторых условиях взаимодействия с поверхностным покрытием, может образовывать сульфид хрома, который, в свою очередь, ведет к быстрому окислению. [41]
Они представляют собой аморфные осадки, практически не растворимые в воде, но способные давать коллоидные растворы. Сульфиды хрома и алюминия, получаемые сухим путем, вследствие своей сравнительно хорошей растворимости полностью гидролизуются водой. [42]
Сггп обозначают промежуточный трехвалентный ион хрома и катионную вакансию в сульфиде хрома. Символы 0 и ф обозначают квази-свободный электрон в решетке и электронную дырку. Сульфид хрома является полупроводником р-типа с дефицитом металла и имеет катионные вакансии. [43]
Сульфид хрома плохо реагирует с кислотами, но окисляется азотной кислотой, царской водкой или расплавленными нитратами щелочных металлов. В результате нагревания в токе водорода Cr S3 восстанавливается до CrS. Сульфид хрома служит катализатором гидрогенизации ненасыщенных углеводородов и ароматических нитропроизводных. [44]
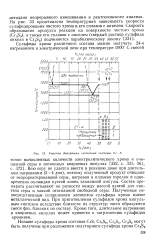 |
Участок диаграммы состояния системы Сг-S. [45] |
Страницы: 1 2 3 4