Клеточная суспензия
Cтраница 2
Одна из трудностей измерения электропроводности клеточных суспензий состоит в том, что ток проходит не только через клетку, но также и вомруг нее. Этот источник ошибок устраняется применением уравнения Максвелла, которое выражает сопротивление суспензий из проводящих шариков в проводящей суспензии. [16]
Чтобы решить эту проблему, клеточную суспензию пропускают с высокой скоростью параллельно поверхности мембраны ( рис. 16.7, Б), так что через мембрану за один раунд проходит только небольшая часть циркулирующей жидкости. Остальная ее часть очищает мембрану от накопившихся клеток ( см. рисунок), и в результате скорость фильтрации падает не так быстро, как при необратимом забивании фильтра. После многочисленных раундов фильтрации через мембрану проходит почти вся культуральная среда. Этот метод используется пока только в лаборатории; в промышленных процессах для сбора клеток применяют центрифугирование. [17]
При гомогенизации под высоким давлением концентрированную клеточную суспензию продавливают через небольшое отверстие под высоким давлением, а затем давление резко сбрасывают, что и вызывает лизис. Условия обработки можно оптимизировать применительно к разным микроорганизмам. Для этого изменяют рабочее давление, размер и форму отверстия, температуру клеточной суспензии, число продавлива-ний. [18]
Ряд частичных успехов связан с исследованием клеточных суспензий клеток лимфатических узлов. [19]
Другие условия формирования ЦРК связаны с автолизом клеточных суспензий, типичным для стареющих микробных культур. В силу генетически детерминированной гетерогенности микробных популяций клетки культуры обладают различной чувствительностью к действию как факторов d1; так и факторов d2, индуцирующих автолиз. При этом из автолизирующихся клеток одной части популяции ( чувствительных к индукции автолиза) высвобождаются внутриклеточные факторы d1; что повышает их общий концентрационный уровень в среде. По достижении определенного концентрационного порога факторы dx индуцируют формирование ЦРК клетками другой части популяции, устойчивыми к автолизу. [20]
В сосудики разной величины помещают одинаковые объемы клеточной суспензии. Поглощение света и условия перемешивания в обоих сосудиках также одинаковы. [21]
Оптимизация всех перечисленных выше параметров позволяет получить клеточную суспензию, плотность которой на 4 - е сутки культивирования составляет 6 2x108 клеток / мл. [22]
Дрэпера: спектр отбрасывается на растение или клеточную суспензию и фотосинтез измеряется в различных участках спектра, с выделением полос одинаковой ширины. Подобный эксперимент, проведенный с применением призмы и искусственного источника света, легко может привести к убеждению, что спектр действия фотосинтеза имеет только один максимум, потому что энергия большинства искусственных источников света быстро уменьшается к фиолетовому концу спектра, тогда как дисперсия призмы увеличивается в том же направлении. Совместное действие обоих факторов вызывает быстрое понижение выхода фотосинтеза ( отнесенного к данной ширине спектральной полосы) по мере продвижения от красного к фиолетовому участку спектра, и этого понижения может оказаться более чем достаточно, для того чтобы замаскировать некоторое повышение выхода, вызванное новым подъемом поглотительной способности хлорофилла в сине-фиолетовой области. [23]
Незначительное число комплексных исследований по оценке физико-химических характеристик клеточных суспензий затрудняет теоретические расчеты различных процессов концентрирования. При разработке и подборе способа концентрирования чаще всего пользуются эмпирическими или полуэмпирическими подходами. [24]
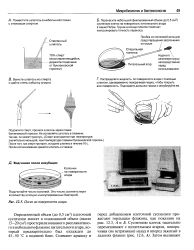 |
Посев на поверхность агара. [25] |
Определенный объем ( до 0 5 см3) клеточной суспензии вносят в подходящий объем ( около 15 - 20 см3) простерилизованного расплавленного в небольшом флаконе питательного агара, который предварительно был охлажден до 45 - 50 С в водяной бане. [26]
Таким образом, негомогенности нельзя избежать, даже применяя разбавленные клеточные суспензии, в которых освещенность одинакова для всех клеток, но не для всех молекул хлорофилла. [27]
О развитии автолитических процессов часто судят по падению оптической плотности клеточных суспензий. Однако более корректно характеризовать автолиз по биохимическим показателям: с одной стороны, высвобождению в инкубационную среду продуктов деградации клеточных биополимеров, липидов, с другой, - снижению их содержания в клетке. [28]
Превращение в CN - кобаламин достигают обрабатывая горячий раствор или клеточную суспензию цианидом или тиоцианатом, часто в присутствии NaNO2 или хлорамина В. Корриноиды сорбируют на различных носителях: амберлите IRC - 50, АЬ Оз, активированном угле и элюируют водными спиртами или водно - фенольными смесями. [29]
 |
Йенициллиновый метод, применяемый для накопления и выделения ауксотрофных мутантов Escherichia coli или других бактерий, чувствительных. [30] |
Страницы: 1 2 3 4