Существование - комплекс
Cтраница 3
Вычислено при допущении существования тетрамминового комплекса при высоких концентрациях аммиака. [31]
Для доказательства возможности существования нитратно-ро-данпдных комплексов был изучен также состав органической фазы при экстракции иттербия 0 26 М раствором HSCN в МЭК в зависимости от концентрации NH NOs в водной фазе. [32]
Лигандная изомерия обусловлена существованием комплексов с изомерными формами лиганда. [33]
Вместе с тем доказано существование комплексов этого типа и в кристаллическом состоянии, например, [ Pt ( NH3) - C2H4 ] Cl; CuCl - C2H4; Н § С1а - С Ная. [34]
Предполагают, что продолжительность существования комплекса [ АВ ] в твердой фазе велика. Вследствие этого комплекс [ АВ ] находится в тепловом равновесии с окружающей средой. [35]
Установленный недавно [120] факт существования комплексов ДФПГ с растворителями может заставить несколько пересмотреть значения скоростей инициирования, полученные ранее при помощи этого соединения. [36]
Для Rh спектрофотометрическим методом установлено существование комплекса о ЭДТА [ 58 ( 78) ], который получен также препаративным путем, но до настоящего времени ничего не известно о его аналитическом применении. [37]
В большинстве работ [2, 11, 13] предполагается существование катализирующего комплекса с металлом на основании кинетических данных; в некоторых, в частности у Робинса [12], на основании изучения теплоты реакции изоцианат - гидроксил в присутствии катализирующего иона. Единственная известная нам работа [3], в которой при изучении каталитического действия металла ( окиси и ацетата цинка) были выделены катализирующие соединения в виде алкоголятов, посвящена исследованию исходной гетерогенной системы. [38]
Для ZnH2L этой стадии предшествует существование устойчивого безводного комплекса в интервале 150 - 210 С. Для двух других комплексов процесс разложения начинается сразу после дегидратации. Последующая деструкция молекулы всех комплексов протекает со значительными экзотермическими эффектами. [39]
Для ZnH2L этой стадии предшествует существование устойчивого безводного комплекса в интервале 150 - 210 С. Для двух других комплексов процесс разложения начинается сразу после дегидратации. Последующая деструкция молекулы всех комплексов протекает со значительными экзотермическими эффектами. [40]
Принимая во внимание доказанную возможность существования комплексов с молекулой соли, находящейся во внутренней сфере ( например, типа [ Pt2NH3SCN ( SCNAg) ] N03, также соль Вильма), нельзя отрицать принципиальную возможность существования подобных соединений, но все же трудно рассчитывать получить именно данные соединения, содержащие координированную молекулу амида натрия. [41]
Как уже говорилось, реальность существования комплексов некоторых металлов с азотом была недавно показана, причем интересно, что и моно - и биметаллические комплексы могут образовываться в присутствии воды. [42]
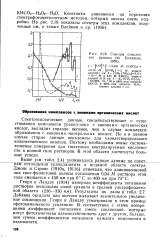 |
Спектры комплексов уранила ( по Комарову, 1959. [43] |
Спектроскопические данные, свидетельствующие о существовании комплексов уранил-иона с анионами органических кислот, выглядят гораздо весомее, чем в случае комплексо-образоваиия с анионами минеральных кислот. Но и в данном случае старые данные ненадежны для удовлетворительного количественного анализа. Поэтому необходимы новые систематические измерения при тщательно контролируемых кислотности и ионной силе растворов. В этой области достигнуты большие успехи. [44]
Страницы: 1 2 3 4