Существование - ионные пары
Cтраница 1
Существование ионных пар подтверждено спектрофотометр ически-ми исследованиями растворов, методами ЭПР и ЯМР. [1]
Существование ионных пар подтверждено спектрофотометриче-скими исследованиями растворов, методами ЭПР и ЯМР. [2]
Существование ионных пар должно сказаться при рассмотрении деталей влияния двойного слоя на кинетику электродного процесса; поэтому представлял бы интерес соответствующий пересчет некоторых опубликованных данных. [4]
Схема предусматривает существование ионных пар разного типа тесно и рыхло связанных. В последних ионы отделены друг от друга сольватной оболочкой, что на схеме показано двумя черточками. Следовательно, помимо ионов и молекул, существуют образования промежуточного типа. Они более близки либо к молекулам, либо к свободным ионам. [5]
Для доказательства существования ионных пар использовали кинетический и стереохимический методы. [6]
Представление о существовании ионных пар в растворах было впервые развито в 1925 г В. [7]
Одним из доказательств существования ионных пар в органических растворителях являются высокие значения дипольных моментов растворов ониевых солей. Возможно, что столь большие дипольные моменты способствуют образованию каталитического комплекса с другим реактантом, перестройка которого приводит к продуктам реакции. В то же время большие дипольные моменты ионных пар приводят к изменению диэлектрической проницаемости раствора и тем самым к изменению скорости реакции. [8]
Таким образом, предположение о существовании ионных пар удовлетворительно объясняет различия в кинетическом поведении сильных и слабых кислот. Возможно также существование промежуточных случаев. [9]
В 1958 г. Вайсман получил физические доказательства существования ионных пар различного типа при изучении ЭПР-спек-тров нафталиннатрия. [10]
Интересно проанализировать, каким образом были получены экспериментальные доказательства существования ионных пар различного типа и свободных ионов. [11]
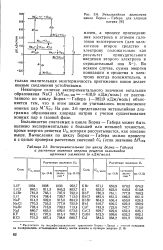 |
Энтальпийная диаграмма.| Экспериментальные ( по циклу Борна - Габера. [12] |
На рис. 3.6 представлена энтальпийная диаграмма образования хлорида натрия с учетом существования ионных пар в газовой фазе. [13]
В заключение отметим, что материал, представленный в книге, не только доказывает существование ионных пар, но и наполняет это понятие конкретным содержанием и наглядностью. [14]
Однако нельзя считать полностью доказанным, что именно ассоциация ионов в смешанных водно-органических системах обеспечивает четкие изломы на кривых титрования некоторых ионов, так как существование предполагаемых ионных пар в рассмотренных примерах не подтверждено современными физическими и физико-химическими методами исследования. Кроме того, не учтено, что перхлораты и некоторые другие соли щелочных металлов хорошо диссоциируют в ДМСО, отличающимся высокими сольвати-рующими свойствами и легко образующим с водой и солями комплексы. И, наконец, полностью игнорируется равновесие, устанавливаемое между контактными ( тесными) и сольватно-разде-ленными ( рыхлыми) ионными парами. [15]
Страницы: 1 2