Существование - ионные пары
Cтраница 2
Следует иметь в виду, что ассоциации подвергаются сольвати-рованные ионы. Существование ионных пар доказано различными экспериментальными методами - измерением электропроводности, ЭД С и др. Образование ионных пар может сопровождаться как полной или частичной десольватацией ионов, так и неизменностью сольватных оболочек. Ионные пары имеют высокие дипольные моменты. [16]
В ионите возможно существование ионов: в виде свободного электролита, в диффузионном слое Гун, в плоском слое Гельм-гольца. Возможно также существование ионных пар и хемосорби-рованных ионов, образовавших с функциональной группой малодиссоциированное соединение. [17]
Достаточно сильно взаимодействовать с окружением могут не только ионы, но и ионные пары. Известно, что само существование ионных пар обязано сильной поляризации среды. [18]
Достаточно сильно взаимодействовать с окружением могут не только ионы, но и ионные пары. Известно, что само существование ионных пар обязано сильной поляризации среды. Это взаимодействие может обеспечить достаточно большое число сильно связанных с протоном осцилляторов N и высокие значения Q и AQ. Что же касается величины S, то оценка ее представляется затруднительной. Модель двойной симметричной потенциальной ямы для протона здесь едва ли применима. В самом деле, реакцию образования ионной пары R АН - - 8 j RA - - - HBRi, по-видимому, нельзя сводить просто к переходу протона, как это часто делается в литературе. Главную роль играет, по всей вероятности, ориентационнаяполяризация. Последняя, как известно, много медленнее, чем движение протона ( характеристические времена равны соответственно 10-и - 10 - 12 и 10 - 13 - 10 1 сек. Поэтому скорость реакции определяется не столько его движением, сколько реорганизацией растворителя, и модель протонного адиабатического терма для реакции АН - - В - А - - - НВ не законна. Соответствующая энергетическая диаграмма показывает изменение энергии всей системы ( протон-растворитель) в зависимости от некоторой обобщенной координаты, относящейся к растворителю и к протону. При этом, в частности, не может происходить туннелирования протона из одной ямы в другую. [19]
Особенно много внимания ионной ассоциации было уделено в химии карбанионов и анион-радикалов. Здесь с помощью различных физических методов исследования были получены прямые доказательства существования ионных пар различного типа. [20]
Мы не будем здесь касаться вопросов, связанных с применением к комплексным ионам учения об активности, поскольку в этом отношении комплексные ионы не характеризуются какой-либо особой спецификой по сравнению с так называемыми простыми ионами. Однако укажем на то, что в ряде случаев и для комплексных ионов удалось установить существование ионных пар, которые могут отчетливо сказываться как на термодинамических, так и на кинетических свойствах комплексных ионов. [21]
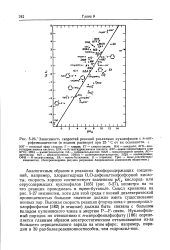 |
Зависимость скоростей реакций различных нуклеофилов с п-нит. [22] |
Аналогичным образом в реакциях фосфорсодержащих соединений, например, хлорангидрида О О-дифенилтиофосфорной кислоты, скорость хорошо соответствует значениям р / С0 кислород - или серусодержащих нуклеофилов [185] ( рис. 5 - 27), несмотря на то что реакция проводилась в / npem - бутаноле. Смысл кривизны на рис. 5 - 27 неизвестен, хотя для этой среды с низкой диэлектрической проницаемостью большое значение должно иметь существование ионных пар. Высокая скорость реакции фторид-иона с диизопропил-хлорфосфатом [182] ( в этаноле) должна быть связана с большим вкладом кулоновского члена в энергию Р - F - связи. Нуклеофиль-ный порядок по отношению к / г-нитрофенилфосфату [186] определяется главным образом электростатическим отталкиванием из-за большего отрицательного заряда на этом эфире; например, пиридин в 30 раз более реакционноспособен, чем гидроксил-ион. [23]
Истинные электролиты могут существовать в растворе в виде равновесной смеси ионных пар и свободно сольватированных ионов. Ионной парой называют два разноименно заряженных иона с общей сольватной оболочкой. В растворах электролитов существование ионных пар как индивидуальных частиц можно обнаружить экспериментально путем изучения электропроводности, кинетики некоторых процессов и при определении ряда термодинамических параметров, например коэффициентов активности, осмотического давления. [24]
Однако образование ионной пары, сопровождаемое внутренним возвратом, может оказывать влияние и на стереохимию молекулы субстрата RX. Показано, что в некоторых случаях, когда в результате внутреннего возврата происходит рацемизация, она идет быстрее сольволиза. Это также служит доказательством существования ионных пар. [25]
Таким образом, о механизме данной перегруппировки нет еще достаточно надежно подтвержденного единого мнения. В настоящем сообщении изложены результаты исследования кинетики гетеролитической перегруппировки кумилпербензоата и некоторых его производных. Особое внимание при этом обращено на зависимость скорости реакции от природы заместителя в перэфире и от ионизирующей силы среды, а также от природы катализатора. Одновременно с этим было проведено масс-спектрометрическое исследование с целью установления существования ионных пар в реакциях перегруппировки перэфиров. [26]
Страницы: 1 2