Существование - твердая фаза
Cтраница 2
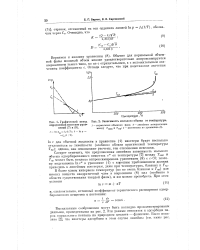 |
Графический метод [ IMAGE ] Зависимость мольного объема от температуры. [16] |
В более узком интервале температур ( но не очень близком к Тк) для многих веществ квадратичный член в выражении ( 8) мал ( особенно в области существования твердой фазы), и им можно пренебречь. [17]
Эти данные представляют интерес потому, что отпускной хрупкости оказалось подверженным кремнистое железо с примесью фосфора ( Fe 2 5 % Si 0 06 % Р), имеющее ОЦК решетку, т.е. представляющее собой а-раствор, во всей температурной области существования твердой фазы. Следовательно, специфическое влияние примесей на развитие обратимой отпускной хрупкости не связано с особенностями их растворимости и сегрегации на границах зерен в аустените. Результаты этого исследования показали, что принципиально те же процессы обогащения границ зерен фосфором возможны в феррите, не содержащем границ исходного аустенитного зерна. [18]
 |
Диаграмма плавкости системы медь-никель ( по Н. С. Курнакову и С. Ф. Жемчужному. [19] |
Выше кривой ликвидуса на рис. 45 расположена область существования жидкой фазы. Ниже кривой солидуса находится область существования твердой фазы. Между кривой ликвидуса и кривой солидуса лежит область температур и составов, при которых жидкая фаза сосуществует с твердой. [20]
 |
Диаграмма плавко. [21] |
Выше кривой ликвидуса на рис. 45 расположена область существования жидкой фазы. Ниже кривой солидуса находится область, существования твердой фазы. Между кривой ликвидуса и кривой солидуса лежит область температур и составов, при которых жидкая фаза сосуществует с твердой. [22]
Существующие в системе фазы зависят от температуры и состава В рассматриваемой системе существуют лишь две фазы: жидкая и твердая. Линия TQeXTSi представляет собой верхнюю границу температурной области существования твердой фазы, а линия TGeYTst - нижнюю границу жидкости. [23]
В кристалле мы имеем нечто подобное: переходы от [ С ] к [ C4F ] и далее к [ CF ] скачкообразны, но ввиду того, что макроскопический кристалл представляет собой нечто единое, структура всего целого может тем или иным способом достигать определенной, специфической характеристики еще задолго до того, как будет достигнуто ( с той или иной стороны) строго стехио-метрическое соотношение компонентов. Таким образом, в ряде случаев может быть объяснено существование твердых фаз переменного состава. [24]
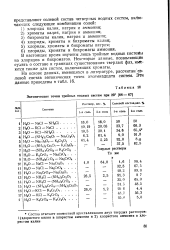 |
Эвтонические точки тройных водных систем при 20. [25] |
В настоящее время изучены лишь тройные водные систейы из хлоридов и бихроматов. Некоторые данные, позволяющее судить о составе и границах существования твердых фаз, имеются также для систем, включающих хроматы. [26]
Химических соединений в равновесии с насыщенным раствором может быть несколько. На рис. 66, в приведена политермическая диаграмма пределов существования твердых фаз в контакте с насыщенными растворами, позволяющая проследить порядок выделения различных соединений по мере изменения температуры. [27]
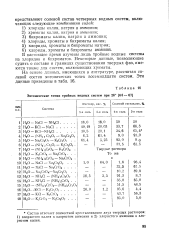 |
Эвтонические точки тройных водных систем при 20. [28] |
В настоящее время изучены лишь тройные водные системы из хлоридов и бнхроматов. Некоторые данные, позволяющие судить о составе и границах существования твердых фаз, имеются также для систем, включающих хроматы. [29]
Диаграмма состояния, приведенная на рис. V.4, интересна тем, что она иллюстрирует заметное влияние устойчивости соединения SiO на форму кривых давления пара. Резкое увеличение давления пара вблизи состава SiO соответствует узкой области существования твердой фазы. Фактически этот пик аналогичен пикам, образующимся на диаграммах состояния в области существования конденсированных фаз. В обоих случаях резкое увеличение давления соответствует большой устойчивости соединения. [30]
Страницы: 1 2 3