Координационные сферы
Cтраница 2
Он образует октаэдрические и тетраэдриче-ские координационные сферы. Они образуются только в концентрированных растворах и окрашивают их в синий или фиолетовый цвет. [16]
После перекрытия координационных сфер должна уменьшаться конфигурационная энтропия отдельных цепей. Действительно, из-за помех, вносимых соседними цепями, число степеней свободы контактирующих участков макромолекул уменьшается, и они вынуждены располагаться параллельно. В работах ДиМарцио 57 60 этот вопрос анализируется с позиций статистической механики для модели жестких цепей. Жесткие цепи расположить в ограниченном объеме в полном беспорядке труднее: выигрыш в термодинамическом потенциале смешения может быть достигнут за счет энтропии ( как и около НКТС, но по другой причине), и равновесным окажется состояние, в котором растворенные молекулы ориентированы параллельно. Подробно этот вопрос был рассмотрен Флори 61, а ДиМарцио придал его расчетам более строгий характер. [17]
Для обозначения координационных сфер применяются квадратные скобки. [18]
Выразим радиусы координационных сфер rk через радиус г первой сферы ri, r 8k, где коэффициенты 8k однозначно определяются типом кристаллической структуры и не зависят от размера элементарной ячейки кристалла. [19]
Катион Сг3 образует прочные координационные сферы со многими монодентатными лигандами, в том числе с тиоциа-нат-ионами SCN -, фторид-ионами F -, молекулами аммиака NH3, а также с разнообразными полидентатными лигандами. Все эти координационные сферы кинетически инертны: они медленно образуются и медленно диссоциируют. Для Сг3 характерно образование многоядерных комплексов, в которых SCN и NH3 могут служить мостиками между атомами хрома. [20]
У таких структур ближайшие координационные сферы чаще всего сохраняются. Политипы слоистых материалов обозначают преим. В то же время для политипов можно предсказывать теоретически все мыслимые модификации, а для полиморфных модификаций этого сделать нельзя. [21]
Дальнейшее увеличение числа координационных сфер должно привести к размытию упомянутых уровней в зоны. [23]
Высока также устойчивость координационных сфер, в которых имеются лиганды с донорными атомами углерода, азота, фосфора и серы. [24]
Различают два типа координационных сфер: открытые и закрытые. В открытых структурах ион металла не экранирован полностью лигандами и доступен извне. Типичны два ряда открытых конфигураций: плоские правильные многоугольники с атомом металла в центре и правильные пирамиды с атомом металла в вершине. Лиганды в них сближены сильнее, чем в правильных многогранниках с тем же КЧ. [25]
Состав и строение координационных сфер координационных полимеров определяется на основании результатов изучения химических свойств полимера, измерения молекулярного веса в органических растворителях, молекулярной электропроводности растворов или хроматографичеоким методом. [26]
Роль мостиков, соединяющих координационные сферы многоядерных комплексов, могут играть самые различные молекулы и атомы. [27]
Типичные для различных катионов координационные сферы показаны в табл. 23.7. Для многих катионов характерно существование геометрически различных координационных сфер. Этот факт очень важен, так как координационные сферы, имеющие разную форму, но примерно одинаковую устойчивость легко обмениваются лигандами. [28]
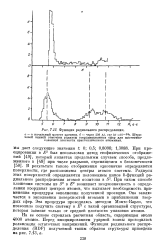 |
Функция радиального распределения. [29] |
Штриховой линией отмечены радиусы координационных сфер для плотноупа-кованной плоскости кристаллического алюминия. [30]
Страницы: 1 2 3 4