Схема - линдеман
Cтраница 1
Схема Линдемана не только позволяет объяснить переход кинетики первого порядка в кинетику второго порядка с изменением давления, но и дает аналитическую зависимость константы скорости от давления. [1]
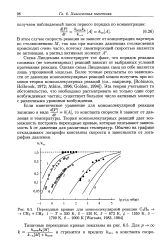 |
Переходные кривые для мономолекулярной реакции С2Нв . [2] |
Схема Линдемана иллюстрирует тот факт, что порядок реакции сложных ( не элементарных) реакций зависит от выбранных условий протекания реакции. Однако схема Линдемана сама по себе является лишь упрощенной моделью. Эта теория учитывает то обстоятельство, что необходимо рассматривать не только один сорт возбужденных частиц; существует большое число активных молекул с различными уровнями возбуждения. [3]
Схема Линдемана объяснила наблюдающуюся на опыте смену порядков реакции с изменением давления. Время полураспада обратно пропорционально константе скорости реакции; с ростом давления значения Л /, уменьшаются, достигая постоянного значения. Обнаружено, что в процессах активации и дезактивации молекул реагента А участвует не только сам реагент. Важную роль в некоторых случаях играют продукты реакции и посторонние газы. Эффективно участвуя в процессах передачи энергии, водород компенсирует влияние уменьшения начального давления эфира и поддерживает период полураспада на уровне, отвечающем высоким начальным давлениям эфира. Часто подобным компенсирующим влиянием обладают продукты реакции, поэтому наблюдаемая мономолекулярная константа скорости реакции / сэф не изменяется в ходе опыта, даже если давление реагента сильно уменьшается. [4]
Схема Линдемана позволяет не только объяснить переход кинетики первого в кинетику второго порядка с изменением давления, но дает и аналитическую зависимость константы скорости от давления. [5]
Согласно схеме Линдемана, газофазные реакции как первого, так и второго порядка происходят в результате молекулярных столкновений. [6]
Согласно схеме Линдемана, принципиальной разницы между мономолекулярным и бимолекулярным механизмами реакций нет. Все различие между ними состоит в соотношении между временем жизни активного комплекса и промежутком времени между столкновениями. Для двухатомных и трехатомных молекул ( например, J2, NOC1, NO2), у которых вся энергия, подученная при столкновении, сосредоточивается на одной-двух связях, время жизни активного комплекса мало и распад осуществляется еще до того, как молекула успевает дезактивироваться в результате столкновения. Поэтому реагируют все активированные столкновениями молекулы, и выполняется кинетическое уравнение второго порядка. Однако и здесь, по крайней мере теоретически, при резком увеличении давления возможен переход к кинетике реакции первого порядка. Для сложных молекул переход к кинетике второго порядка оказывается возможным лишь при возрастании времени между столкновениями до величин, значительно больших, чем время жизни активного комплекса ( см. § 9, гл. III), что и осуществляется при понижении давления до величины, характерной для каждой данной молекулярной системы. [7]
Согласно схеме Линдемана принципиальной разницы между мономолекулярным и бимолекулярным механизмами реакций нет. Все различие между ними состоит в соотношении между временем жизни активного комплекса и промежутком времени между столкновениями. Для двухатомных и трехатомных молекул ( например, z, NOC1, NO2), у которых вся энергия, полученная при столкновении, сосредоточивается на одной - двух связях, время жизни активного комплекса мало и распад осуществляется еще до того, как молекула успевает дезактивироваться в результате столкновения. Поэтому реагируют все активированные столкновениями молекулы и выполняется кинетическое уравнение второго порядка. Однако и здесь, по крайней мере теоретически, при резком увеличении давления возможен переход к кинетике реакции первого порядка. Для сложных молекул переход к кинетике второго порядка оказывается возможным лишь при возрастании времени между столкновениями до величин, значительно больших, чем время жизни активного комплекса ( см. § 9, гл. III), что и осуществляется при понижении давления до величины, характерной для каждой данной молекулярной системы. [8]
Таким образом, схема Линдемана позволяет объяснить, как механизм активации, так и причины перехода мономолекулярных реакций при низких давлениях в реакции второго порядка. [9]
Таким образом, схема Линдемана позволяет объяснить как механизм активации, так и причины перехода мономолекулярных реакций при низких давлениях в реакции второго порядка. [10]
Таким образом, согласно схеме Линдемана [ уравнение ( VII. Надо сказать, что IKO времени опубликования схемы подобной зависимости известно не было, но специально поставленные исследования показали ее действительное существование. [11]
Проведенное рассмотрение показывает, что, несмотря на отклонения от схемы Линдемана - Хиншельвуда, закономерности термической цыс-гранс-изомеризации можно объяснить на основе теорий мономолекулярных реакций, предполагающей активирование за счет соударений двух молекул. [12]
Несмотря на изложенное выше соответствие ( хотя более качественное) схемы Линдемана к приведенных опытных данных, все же в целом она оказалась неудовлетворительной. [13]
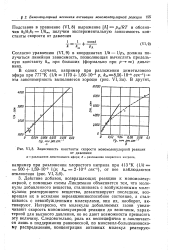 |
Зависимость константы скорости мономолекулярной реакции. [14] |
Действие добавок, возвращающих реакцию к мономолекулярной, с помощью схемы Линдемана объясняется тем, что молекулы добавленного вещества, сталкиваясь с возбужденными молекулами реагирующего вещества, дезактивируют последние, возвращая их в исходное нереакционноспособное состояние, а сталкиваясь с невозбужденными молекулами, они их, наоборот, активируют. Интересно, что молекулы добавляемых газов увеличивают скорость мономолекулярной реакции до величины, характерной для высокого давления, но не дают возможности превысить эту величину. [15]
Страницы: 1 2