Схема - механизм - реакция
Cтраница 3
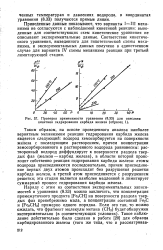 |
Проверка применимости уравнения для описания кинетики гидрирования карбида железа ( образец 1. [31] |
Приведенные данные показывают, что варианты I-III механизма не согласуются с наблюдаемой кинетикой реакции: выведенные для соответствующих схем кинетические уравнения не описывают экспериментальные данные. Соответствие кинетического уравнения, выведенного для гипотетической схемы механизма, и экспериментальных данных получено в единственном случае для варианта IV схемы механизма реакции при третьей лимитирующей стадии. [32]
Карбонильная группа чвлается одной из наиболее распространен-ных функциональных групп; поэтому исследованию реакций карбонильных групп е органическом синтезе и механизмов этих реакций придает ся большое значение. В двух первых главах книги 2 подробно рассмотрена химия карбонильных соединений, отражающая значимость карбонильной группы в органическом синтезе, В этой главе основным предметом обсуждения будут типичные схема механизмов реакций по карбонильным центрам. [33]
Опубликованные в 1947 г. работы американских ученых, касающиеся механизма окислительного нитрования бензола56 - 57, показывают, что эти исследователи, применяя несколько иные методы, дают такую же схему механизма реакции, к какой ранее пришли советские исследователи. [34]
Якобсен, Роберте и Савьер [62] изучили окисление формиата в диметилсульфоксиде на золотом и платиновом анодах методами хронопотенциометрии, кулонометрии, циклической вольтамперомет-рии и выполнили химический анализ продуктов. Реакция, в которой по кулонометрическим данным участвует несколько больше одного электрона на 1 моль, дает двуокись углерода и ионы водорода. Схема механизма реакции, представленная уравнениями (4.28) - (4.30), объясняет образование получившихся продуктов и результаты кулонометрических измерений. [35]
Реком-ендуя эту книгу читателю, мне хотелось бы еще раз предупредить, что здесь не содержится весь объем знаний, который нужен учащемуся. Работа с этой книгой не освобождает от работы с учебником, но многим она эту работу облегчит. Механизмы, точнее схемы механизмов реакций, которые использует А. Е. Агрономов, не всегда доказаны для отдельных, специфических условий и просто могут расходиться с экспериментально установленными. Впрочем, для всех основных процессов, которые рассматривает автор, его толкование не расходится с интерпретацией других авторов учебных пособий нашего времени. При углубленном изучении выявляется, что некоторые процессы, описанные схематически просто, в действительности протекают значительно сложнее и механизм их неоднозначен. Но представления, которые дает А. Е. Агрономов, оказываются достаточно верными для первичной ориентировки. Например, реакции электрофильного замещения в ароматическом ряду в этой книге, как в большинстве учебников органической химии, рассматриваются как процессы, идущие последовательно через стадии я - и затем ст-комплекса. Однако есть серьезные основания полагать ( а для некоторых случаев уже и прямая информация), что такие процессы могут идти с первоначальным переносом одного электрона и образованием комплексов с переносом заряда. Эта новая концепция значительно дополняет и углубляет наши представления, иногда даже отвергает старые, однако не снимает возможность получить при использовании старой теории достаточно точное совпадение с экспериментом. [36]
В условиях 350 - 450 С и времени контакта 0 1 - 0 5 сек ими проводилась дегидратация бутанола - - 2, октанола-2, 4-метилпентанола - 2 и Ьциклогвксилэта-нола. Катализаты этих спиртов содержали 93 - 987о а-олефинов и только 2 - 7 % р-олеф инав. Авторы [462] предлагают схему механизма реакции, из которой не ясно, почему именно водород метильной группы должен преимущественно хемосорбироваться на кислородных атомах катализатора, чтобы в: результате выделения воды образовался а-олефин. [37]
Исключение концентраций промежуточных веществ из кинетических уравнений в случае, когда механизм реакции содержит нелинейные стадии, может оказаться неосуществимым. Это, однако, не является непреодолимым препятствием для сопоставления гипотезы о механизме реакции с опытом. В сущности, если задана схема механизма реакции, то тем самым задана в неявной форме и ее кинетика. Как показано в докладе Малкина, Островского и Снаговско-го на этом Симпозиуме [19], при современном состоянии электронной вычислительной техники такое задание кинетики достаточно, так что можно обойтись без алгебраического решения системы уравнений, выражающих закон действующих масс и условия стационарности. [38]
Надо отметить, что существующие теории объясняют механизмы реакций медленного окисления углеводородов в основном при помощи реакций радикалов алифатических углеводородов ( СН3, С. По мнению некоторых авторов, этих реакциях принимают участие радикалы типа RO. Льюис и Эльбе [3] вводят в свою схему механизма реакций медленного окисления также радикал ОН, образование которого они не объясняют. Атомы водорода в схему, невидимому, не вводятся потому, что но известна элементарная реакция, приводящая к их образованию. Наличие пли отсутствие атома водорода и радикала ОН в зоне медленного окисления углеводородов до сих пор никем точно не доказано. Нам кажется, что только тщательное изучение элементарных реакции этих радикалов ( П и ОН), а также реакций других радикалов, например алифатических, поможет разрешить вопрос о роли этих радикалов в механизме окисления. [39]
В рамках развиваемого подхода, изложенного в главе 3, основой для кинетического анализа процесса являются удельные скорости реакции. Удельные скорости топохимической реакции представляют собой стационарные величины, так что дальнейший анализ, в том числе и анализ механизма, может быть проведен при использовании классических приемов. Как известно, кинетические данные не всегда дают возможность однозначного выбора схемы механизма реакции, однако получаемая из них информация о механизме значительна и обычно не дублируется другими методами исследования. [40]
Монография Питера Сайкса не нуждается в многословном представлении. Она уже выдержала шесть изданий и переведена на многие языки. Книга имеет широкую читательскую аудиторию, поскольку сложные понятия теоретической органической химии и схемы механизмов реакций большинства классов органических соединений автор излагает лишь на основе выдержавших испытание временем концепций. Оставаясь верным, как и в предыдущих изданиях, электронным представлениям, Питер Сайке при интерпретации богатейшего экспериментального материала ограничивается понятиями, введенными Льюисом, Полингом, Робинсоном, Ингольдом, Хюккелем. [41]
Пиролиз циклогексана с добавками аллена исследован при 620 - 700 С при концентрации циклогексана в гелии 2 - 6 мол. Изучена кинетика термического распада циклогексана в присутствии добавок аллена и предложена схема механизма реакции, в которой стадией инициирования цепей является реакция диспропорциопироваиия аллена с циклогексаном и бу-теном. [42]
Пиролиз циклогексана с добавками аллепа исследован при 620 - 700 С при концентрации циклогексана в гелии 2 - 6 мол. Изучена кинетика термического распада циклогсксана в присутствии добавок аллена и предложена схема механизма реакции, в которой стадией инициирования цепей является реакция диспропорционирования аллена с циклогексаном и бу-тсном. [43]
Уравнение ( 21) позволяет сразу исключить часть неизвестных активностей ( или концентраций) промежуточных веществ, а иногда и все. Для этого нужно расположить уравнения стадий по возможности в таком порядке, чтобы промежуточное вещество, образующееся в какой-либо стадии, расходовалось в следующей стадии. Несколько таких расположений дают нужное число уравнений, равное числу неисключенных неизвестных. Выражения для концентраций промежуточных веществ, если нужно, также могут быть получены с помощью подходящих последовательностей стадий. Если схема механизма реакции содержит равновесные или квази-равновесные стадии, активность участвующего в такой стадии промежуточного вещества находится с помощью закона действующих масс для равновесия. Охарактеризованный здесь в общей форме способ вывода кинетических уравнений будет ниже иллюстрирован примерами. [44]
Рассмотрим теперь - механизм реакции гидрирования карбида железа для этих образцов. Наблюдаемый порядок реакции по водороду для этих образцов близок к единице. Это облегчает анализ, так как можно сразу удостовериться в том, что то или иное кинетическое уравнение не может быть сведено к уравнению первого порядка. К таким уравнениям, например, сразу можно отнести уравнения (8.19), (8.23), (8.26), (8.28), (8.29), (8.33), не сводящиеся к уравнению первого порядка. Число схем механизма реакции, подлежащих рассмотрению, таким образом, существенно уменьшается. [45]
Страницы: 1 2 3 4