Схема - молекулярный орбиталь
Cтраница 1
Схема молекулярных орбиталей для УО ( Н О) 5 -иона. [1]
Схема молекулярных орбиталей приведена ниже. [2]
 |
Оси координат октаэдре. [3] |
Расчет схемы молекулярных орбиталей в методе МО ЛКАО сводится к составлению и решению системы линейных уравнений относительно коэффициентов разложения МО на АО. Если базисный набор АО составлен из N орбиталей, то система уравнений имеет Л - й порядок. Решение таких систем затруднено даже для относительно простых молекул: так, для молекулы SFe учет только внешних s и р-орбиталей атомов серы и фтора приводит к системе из 28 уравнений. [4]
Полученная Коттоном схема молекулярных орбиталей центральной Группировки [ Мо6С18 ] 4 включает двенадцать связывающих МО, отвечающих за взаимодействие между атомами металла, на которых размещается двадцать четыре электрона. Формальная кратность связи М - М ( если говорить об отдельных таких связях) равна, следовательно, единице. В комплексах [ Nb6X12 ] 2 и [ ТавХ12 ] 2 на те же двенадцать связывающих орбиталей приходится только шестнадцать электронов. Уменьшение числа связывающих электронов сказывается на расстояниях. В комплексах Мо и W расстояния М - М лежат в области 2 61 - 2 65 А, в комплексах Nb и Та - в пределах 2 82 - 2 92 А. [5]
На основании схемы молекулярных орбиталей ( см. рис. П-1) и принимая во внимание, что поворот должен приводить к перекрыванию полостей орбиталей с одинаковыми знаками функции, нетрудно вывести, что для шести-я-электронной системы фотохимическое возбуждение должно приводить к конротаторному повороту, а термическое - к дисротаторному. [6]
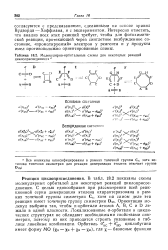 |
Молекулярно-орбитальные схемы для некоторых реакций циклоприсоединения а. [7] |
В табл. 18.2 показаны схемы молекулярных орбиталей для некоторых реакций циклоприсоединения. С целью единообразия при рассмотрении всей реакционной серии димеризация этилена охарактеризована в рамках точечной группы симметрии C. Ориентация молекул выбрана так, чтобы я-орбитали атомов А, В, С и D лежали в одной плоскости. Локализованные а-орбитали в циклических структурах не обладают необходимыми свойствами симметрии, поэтому из них приходится строить указанные в таблице линейные комбинации. [8]
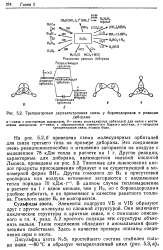 |
Трехцентровая двухэлектронная связь у бороводородов и реакции. [9] |
На рис. 5.2 6 приведена схема молекулярных орбиталей для связи третьего типа на примере диборана. Это соединение очень реакционноспособно и мгновенно загорается на воздухе с выделением 78 кДж тепла в расчете на 1 г. Другие реакции, характерные для диборана, являющегося сильной кислотой Льюиса, приведены на рис. 5.2. Типичные для льюисовских кислот продукты присоединения образует и не существующий в мо-номерной форме ВНз. В данном случае тепловыделение в расчете на 1 г вдвое меньше, чем у ЬЬ, но с бороводородами удобнее работать, и их применяют в качестве ракетного топлива. [10]
Линейные трехатомные радикалы имеют примерно такую же схему молекулярных орбиталей, как и рассмотренные в гл. [11]
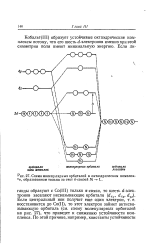 |
Схема молекулярных орбиталей в октаэдрическом комплексе, образованном только за счет ст-связей М - L. [12] |
Со ( 11), то этот электрон займет актисвя-зывающую орбиталь ( см. схему молекулярных орбиталей на рис. 27), что приведет к снижению устойчивости комплекса. [13]
Оставшихся 14 электронов явно недостаточно для образования формально двухэлектронных связей вдоль 12 ребер полиэдра, и, следовательно, вместо них нужно построить схему делокализован-ных молекулярных орбиталей из гибридных spz -, px - и о-орбиталей бора. [14]
Символ я ( 4pz), например, обозначает молекулярную групповую л-орбиталь, которая имеет ту же симметрию, что и 4р2 - орбиталь металла; z / i и z4 - это ру - и / - орбитали первого лиганда; at - это а-орбиталь ( 2s или 2рх) того же лиганда. Схема молекулярных орбиталей, полученных комбинацией орбиталей металла и лиганда, показана на рис. 10.12. Отметим прежде всего, что все связывающие орбитали заполнены и каждая содержит по два электрона. Из них eg, t - iu и tzg локализованы преимущественно на атомах фтора. Кроме того, имеются несвязывающие орбитали ( tig и t2y фтора, которые также заполнены. Более высоко расположенные разрыхляющие орбитали для рассмотрения несущественны. Отметим, что окончательная картина расщепления уровней ( А) в основном такая же, как и в простой электростатической теории, в которой лиганды заменяются точечными отрицательными зарядами, окружающими ион металла. Симметрия, пространственное расположение и принципиальные особенности орбиталей, на которых находятся неспаренные электроны, те же самые, как и в модели кристаллического поля. [15]
Страницы: 1 2