Схема - уровни - энергия
Cтраница 3
Который из семи перескоков, обозначенных стрелками на схеме уровней энергии на рис. 34.7, а, соответствует спектральной линии наименьшей длины волны. [31]
Таким образом, можно заметить некоторые сходства и различие между схемой уровней энергии атома водорода и распределением элементов в периодической системе Менделеева. Если пронумеровать все состояния атома водорода по возрастающим значениям энергии, то соответствующие им квантовые числа п, /, т и 5 будут аналогичны квантовым числам п, /, / и т /, которые определяют положение электронов в сложных атомах. Различия в этих схемах вызваны взаимодействием между электронами, которое отсутствует в атоме водорода, аналогия же обусловлена корпускулярно-волновыми свойствами электронов и общей упорядочивающей тенденцией, направленной ( у сложных систем) к созданию структур с наименьшей возможной энергией. [32]
Графически значения энергии стационарных состояний и квантовые переходы условно изображают при помощи схемы уровней энергии ( см. на стр. На схеме горизонтальные линии проведены на высотах, пропорциональных значениям энергии А. [33]
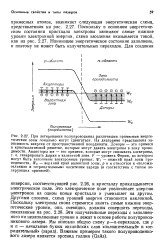
Графически энергию квантовых состояний и квантовые переходы электронов можно изобразить с помощью схемы уровней энергии, как это показано на рис. 1 для электрона атома водорода. На схеме горизонтальные линии проведены на высотах, пропорциональных значениям энергии электрона в атоме, вертикальные указывают на возможные квантовые переходы. [34]
Трофически значения энергии стационарных состояний и квантовые переходы условно изображают при помощи схемы уровней энергии ( см. на стр. На схеме горизонтальные линии проведены на высотах, пропорциональных значениям энергии А. [35]
При небольшом отклонении от симметричного полчка расщепление первоначально вырожденных уровней невелико и мы получаем схему уровней энергии, изображенную справа и слева на фиг. Расщепление уровней совершенно аналогично Л - удвоению в двухатомных молекулах и может быть названо удвоением типа К. [36]
Значения X, приведенные с десятыми долями, получены из анализа структуры, остальные значения - из схемы уровней энергии. [37]
Переходы, приводящие к излучению различных линий в спектре атома водорода, могут быть также изображены на схеме уровней энергии атома. На рис. 50 стрелками показаны переходы, приводящие к излучению линий серии Бальмера, Лаймана и Пашена. [38]
В электрическом разряде атомы испускают свет, и цвет, который мы видим при этом, позволяет определить схему уровней энергии атома. Многоэлектронные атомы, как и атом водорода, испускают линейчатый спектр - можно наблюдать только определенные энергии. Таким образом, для объяснения необходима квантовомеханиче-ская модель. Однако расстояния между уровнями энергии у многоэлектронных атомов не связаны такой простой зависимостью, как уровни атома водорода. [39]
Примесные уровни, приписываемые дыркам, изображены с помощью специального значка, указывающего на то, что энергия дырок растет сверху вниз и что поэтому на схеме уровней энергии дырки имеют тенденцию занять по возможности более высоколежащие энергетические уровни. [40]
Важно отметить, что частота наблюдаемого в спектрах максимума поглощения не имеет четкого физического смысла, так как она сложным образом зависит не только от строения молекулы и характера схемы уровней энергии МО, но и от вероятностных законов поглощения света. [41]
Энергия ионизации равна по абсолютной величине энергии связи электрона в атоме. Схема уровней энергии в атоме водорода показана на рис. VI. Спектр водорода объясняется постулатами Бора. [42]
Если двойная связь и карбонильная группа сопряжены, для описания сложного хромофора требуется иной набор молекулярных орбиталей и уровней энергии, чем для изолированной двойной связи или изолированной карбонильной группы. Схема уровней энергии сопряженного енона представлена ниже. В сопряженном еноне п - я переход сдвинут в длинноволновую область относительно изолированного карбонильного соединения. [43]
На схеме уровней энергии двухатомной молекулы указать разрешенные: а) вращательные; б) колебательно-вращательные переходы. [44]
Страницы: 1 2 3 4 5