Кинетическая схема
Cтраница 4
Рассмотрим кинетическую схему изомеризации цис: цис цис-1 2 3.4 - тетраметилциклогексана. [46]
В кинетической схеме не соответствует действительности исходное положение об образовании второго активного продукта из первого X, например, альдегида из перекиси. Фактически в результате распада перекиси и последующего распада радикала RO можно ожидать только образования формальдегида, как раз не являющегося активным продуктом холоднопламенного процесса. Таким образом, система трех уравнений, решение которой дает периодическую функцию для концентраций предполагаемых активных продуктов, по существу не соответствует природе холодных пламен. [47]
В кинетической схеме, рассмотренной в разд. В возможно только в том случае, если адсорбированный продукт В десорбируется с поверхности в поддающемся обнаружению количестве. Если дальнейшая реакция этого продукта на поверхности с образованием адсорбированного продукта С происходит легче, чем его десорбция, то газообразный продукт В не образуется, хотя он существует в адсорбированном состоянии как промежуточный продукт реакции. В этом случае, когда реакция превращения А в В требует иных каталитических центров, чем конверсия В в С, то если миграция адсорбированного продукта В от центров одного типа к центрам другого типа не происходит, продукт В должен образовываться в газообразном состоянии, хотя бы в столь малых количествах, что они не могут быть определены аналитически. При наличии двух или большего числа различных в химическом отношении центров катализатора система обладает способностью выполнять более чем одну функцию. Реагент А может превращаться в продукт В под действием катализатора X, тогда как дальнейшее превращение В в продукт С может проходить с измеримой скоростью только в присутствии катализатора У. [48]
В кинетической схеме не соответствует действительности исходное положение об образовании второго активного продукта из первого X, например, альдегида из перекиси. Фактически в результате распада перекиси и последующего распада радикала RO можно ожидать только образования формальдегида, как раз не являющегося активным продуктом холодно пламенного процесса. Таким образом, система трех уравнений, решение которой дает периодическую функцию для концентраций предполагаемых активных продуктов, по существу не соответствует природе холодных пламен. [49]
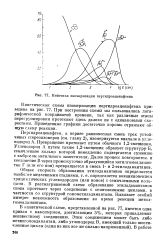 |
Кинетика изомеризации пергидроаценафтена. [50] |
В кинетической схеме, представленной на рис. 77, имеется одна кривая с максимумом, достигающим 5 %, которая принадлежит неизвестному соединению. [51]
В кинетической схеме Томаса и Пеллона сделано допущение о том, что обрыв цепи может происходить также по реакции первого порядка в результате захоронения радикалов. Формально такая модель дает качественно правильное описание некоторых особенностей реакции, однако реальность этого предположения была опровергнута Бемфордом и Дженкинсом [25], которые показали, что доля радикалов, которые должны были бы стать похороненными для подтверждения теории, должна быть значительно больше, чем концентрация застрявших радикалов, наблюдавшаяся в действительности. [52]
В любой кинетической схеме, содержащей замкнутые циклы, условие детального равновесия накладывает связи на константы скорости ( см., например, стр. [53]
 |
Изменение концентрации непрореагировавших групп А во. [54] |
Пользуясь кинетической схемой, аналогичной приведенной выше, Н. А. Платэ теоретически исследовал композиционную неоднородность продуктов полимераналогичных превращений при помощи метода Монте-Карло с использованием электронно-вычислительной техники. [55]
В кинетических схемах, принятых в работах [11, 12], не учитываются обменные реакции. Некоторые исследователи [13] предположили, что протекание этих реакций приводит к сужению ММР по сравнению с законом Флори. Однако теоретическое рассмотрение процесса с учетом этих реакций опровергает возможность такого сужения ММР. Его расчет [14] путем решения соответствующих кинетических уравнений в системе, где протекает только обменная реакция типа алкоголиза или ацидолиза и отсутствуют рост и деструкция макромолекул, приводит к распределению Флори. Рассмотрение общей схемы обратимой гомополиконденсации с учетом роста, деструкции и обменных реакций для мономера с независимыми группами показывает [15], что продукты этого процесса описываются распределением Флори. Кинетическим методом было также-найдено [16] ММР полимера, образующегося при гетерополиконденсации мономеров с функциональными группами различной-активности в одном из них. [56]
Так как кинетическая схема включает только моно - и бимолекулярные реакции, в выражениях для скорости элементарных стадий встречаются произведения не более двух концентраций. [57]
Предложенная авторами кинетическая схема объясняет автоускоренный характер процесса реакцией активных центров с муравьиной кислотой. Последняя в этом случае выступает и в роли инициатора полимеризации, и в роли агента, ускоряющего роста цепи. Эта схема существенно отличается от классической схемы автокатализа в цепных реакциях. Очевидно, что максимальная скорость процесса будет определяться ( по этой схеме) концентрацией кислоты, даже если пренебречь реакцией гибели цепи. [58]
Применима ли данная кинетическая схема для процесса полимеризации триоксана в твердой фазе. [59]
Исходной является следующая кинетическая схема. [60]
Страницы: 1 2 3 4