Амальгама - металл
Cтраница 4
Рассмотрим электрохимический элемент, один из полуэлементов которого составлен из твердого металла Me и его ионов Мега, а второй - из насыщенной двухфазной амальгамы металла Me, находящейся в равновесии с тем же самым раствором. [46]
Сочетая снятую радиохимическим путем анодную кривую с поляризационными кривыми, можно построить кр вую истинной скорости катодного процесса и, следовательно, получить полную поляризационную диаграмму амальгамы металла. Исследования показали, что наиболее медленной стадией процесса анодного растворения амальгамы является ионизация металлического цинка. [47]
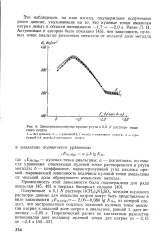 |
Электрокапиллярные кривые ртути в 0 2 N растворе йодистого натрия. [48] |
Вд - нулевая точка амальгамы; а - постоянная, по смыслу уравнения отвечающая нулевой точке растворенного в ртути металла; Ъ - коэффициент, характеризующий угол наклона прямой, выражающей зависимость величины нулевой точки амальгамы от мольной доли образующего амальгаму металла. [49]
Железо может быть амальгамировано также цинковой амальгамой, но лишь в присутствии кислоты, в которой растворяются окислы, образующиеся на поверхности железа. Амальгамы металлов, не имеющих сродства к железу ( свинец, висмут), не амальгамируют его даже при совместном с кислотой действии. [50]
Железо можно амальгамировать также цинковой амальгамой, но лишь в присутствии кислоты, в которой растворяются поверхностные оксиды на же лезе. Амальгамы металлов, не имеющих сродства к железу ( свинец и висмут), не амальгамируют его при совместном с кислотой действии. [51]
В большинстве случаев металл М является элементом побочной группы периодической таблицы. Амальгамы металлов главной подгруппы 1 - й и 2 - й групп разлагаются водой и не находят широкого применения для изучения равновесия. [52]
 |
Аппарат Киппа. [53] |
Для получения водорода часто используются амальгамы металлов. [54]
Ток обмена второй реакции мал и для ведения ее с нужной скоростью требуется уменьшить перенапряжение водорода. Это возможно при осаждении на поверхности амальгамы металла, обладающего низким перенапряжением водорода, малорастворимого в ртути и плохо смачиваемого ею. Как упоминалось выше, такой металл образует микрокатоды, на которых происходит выделение водорода с одновременным переходом натрия из амальгамного электрода в раствор. Таким образом, систему составляет множество гальванических микроэлементов, электродвижущая сила которых Е определяется изменением свободной энергии при взаимодействии натрия с водой. [55]
Страницы: 1 2 3 4