Счет - сольватация
Cтраница 2
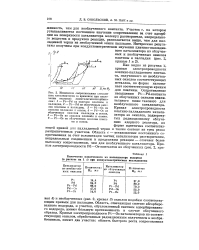
Область с - установление постоянного сопротивления за счет сольватации частиц катализатора растворителем, непредельным соединением и продуктами реакции - отвечает более высокому сопротивлению, чем для необлученного катализатора. [17]
Во всех этих случаях диссоциация HF усиливается за счет сольватации иона водорода молекулами растворенных веществ; очевидно, что концентрация образующихся ионов пропорциональна концентрации растворенного вещества - поэтому формально оказывается возможным вычислять молярную электропроводность растворенного вещества. Предложенный механизм диссоциации приводит к уравнениям процессов электролитической диссоциации, совпадающим с предложенными Фреденхагеном. Не следует забывать, что радикальным отличием от водных растворов большинства веществ является то обстоятельство, что электролитической диссоциации подвергается не растворенное вещество, а растворитель. [18]
Поэтому, вероятнее всего, диссоциация обеспечивается в основном за счет сольватации катиона металла. Метоксид-анион сольвати-руется сравнительно слабо и благодаря этому сохраняет высокую реакционную способность. [20]
Мы видим, что стабилизация мицелл лиофильного золя осуществляется преимущественно за счет сольватации активных групп частиц высокополимера, образующего коллоидный раствор. [21]
Причиной, по-видимому, является то, что последний сильно стабилизирован за счет сольватации гидроксильной группы. [22]
Присутствие кислоты в органической фазе приводит к понижению свободной концентрации экстра-гента ( за счет сольватации) и соответственно - к уменьшению коэффициентов распределения тулия и лютеция. [23]
Вытеснение воды с поверхности металла может происходить в результате ее связывания: за счет сольватации катионами металлов, включения в состав гидратных оболочек гидрофильных составляющих присадок, а также за счет солюбилизации или эмульгирования и стабилизации в виде эмульсий вода - нефтепродукт. [24]
Молекулярное соединение кислоты с основанием ионизируется лишь в результате действия растворителя, которое энергетически обеспечивается за счет сольватации. [25]
Можно представить два типа стабилизирующего действия полимолекулярных слоев: их взаимное отталкивание и снижение поверхностной энергии частиц за счет сольватации до такого уровня, что дисперсная система становится термодинамически устойчивой. Отталкивание реализуется лишь при взаимном перекрывании диффузных сольватных слоев. [26]
Этанол является менее ионизирующим растворителем, чем вода ( см. табл. 8 приложения) и стабилизирует карбоксилат-анион за счет сольватации в меньшей степени, чем вода. [27]
Процесс же растворения высокомолекулярных соединений в низкомолекулярных жидкостях протекает через следующие стадии: 1) набухание высокомолекулярного соединения за счет сольватации макромолекул, 2) набухание высокомолекулярного соединения за счет односторонней диффузии низкомолекулярной жидкости и 3) растворение высокомолекулярного соединения. Таким образом, растворение высокомолекулярного соединения связано с его набуханием. В первой стадии макромолекулы высокомолекулярного соединения покрываются мономолекулярным сольватным слоем низкомолекулярной жидкости. При этом объем высокомолекулярного соединения увеличивается ( происходит его частичное набухание), а объем всей системы ( высокомолекулярное соединение - J - - - растворитель) уменьшается. [28]
В принципе возможны два типа стабилизирующего действия полимолекулярных граничных слоев: их взаимное отталкивание и снижение поверхностной энергии частиц за счет сольватации ( переходный слой) до такого уровня, что дисперсная система становится термодинамически устойчивой. Отталкивание реализуется только при взаимном перекрытии сольватных оболочек, нарушающем их структуру. [29]
Любой способ стабилизации ионов путем делокализации заряда, будь то за счет групп, входящих в состав иона или за счет сольватации, разумеется, тем эффективнее, чем значительнее смещение электронов к катионному центру или от анионного центра. Такая делокализация, однако, не должна переходить некоторые пределы, за которыми происходит разрыв старых или образование новых ковалентных связей. [30]
Страницы: 1 2 3