Таблица - стандартная величина
Cтраница 1
Таблицы стандартных величин позволяют определить Д2, ДЯ и Д5 реакции только при стандартных условиях. Для нахождения этих величин при любой температуре нужно знать зависимость их от температуры. [1]
Из таблицы стандартных величин для СаСО3, СаО и СО2 соответственно находим АЯ. [2]
В таблицах стандартных величин приводятся значения энтальпий и энтропии соединений и элементов. В то время как величины энтальпий относительны ( энтальпия элементов принимается равной нулю), значения энтропии в этих таблицах абсолютны ( см. гл. [3]
В таблицах стандартных величин приводятся значения энтальпий и энтропии соединений и простых веществ. В то время как величины энтальпий относительны ( энтальпия простых веществ принимается равной нулю), значения энтропии в этих таблицах абсолютны ( см. гл. [4]
Существует три вида таблиц стандартных величин: 1) таблицы изменений энтальпии при образовании одного моля вещества при стандартных условиях, 2) таблицы изменений изобарного потенциала образования одного моля вещества при стандартных условиях и 3) таблицы энтропии, рассчитанных на 1 моль вещества при стандартных условиях. [5]
Все подсчеты по таблицам стандартных величин основаны на свойствах аддитивности AZ, ДЯ и S, поэтому сводятся к простому алгебраическому суммированию, аналогичному расчетам по закону Гесса. Так, изменение энтальпии реакции ДЯ равно алгебраической сумме изменений энтальпий при образовании веществ - участников реакции, причем с плюсом берутся продукты реакции, а с минусом - исходные вещества. Это же относится и к AZ и Д5 реакции. Следует заметить, что ДЯ и AZ простых веществ равны нулю, поэтому они в таблицах не помещены. [6]
Все расчеты с помощью таблиц стандартных величин основываются на аддитивном свойстве величин A /, AG, S и поэтому сводятся к простому алгебраическому суммированию по аналогии с расчетами, основанными на законе Гесса. Напомним, что Д / и ДС элементарных веществ приняты равными нулю. [7]
Все расчеты с помощью таблиц стандартных величин основываются на аддитивном свойстве величин ЛЯ, AZ, S и поэтому сводятся к простому алгебраическому суммированию по аналогии с расчетами, основанными на законе Гесса. Напомним, что АЯ и AZ элементарных веществ приняты равными нулю и поэтому они отсутствуют в таблицах. [8]
Рассмотрим некоторые примеры использования таблиц стандартных величин для расчетов равновесий. [9]
Заметим, что в таблицах стандартных величин фигурирует как энтальпия Я - функция, вытекающая из первого закона, так и энтропия S и свободная энергия G, вытекающие из второго закона термодинамики. [10]
Подчеркнем, что в таблицах стандартных величин приводятся АЯ298 образования соединений из элементов, а не из атомов. Например, энтальпия образования Ре3С не равна энергии, которую надо затратить, чтобы разложить это соединение, а затем перевести составляющие его элементы в состояние одноатомных газов. [11]
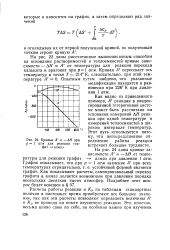 |
Кривые А и - АЯ при р - 1 атм для реакции графит - алмаз. [12] |
Расчеты работы реакции и Кр по таблицам стандартных величин в настоящее время приобретают все большее значение, так как эти расчеты позволяют определить величины А и Кр не проводя на опыте изучаемую реакцию. [13]
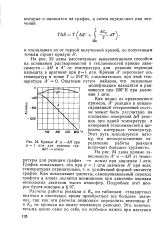 |
Кривые А и - АЯ при р 1 атм для реакции графит - алмаз. [14] |
Расчеты работы реакции и КР по таблицам стандартных величин в настоящее время приобретают все большее значение, так как эти расчеты позволяют определить величины Аг и / Ср не проводя на опыте изучаемую реакцию. [15]
Страницы: 1 2 3