Таблица - термодинамическая функция
Cтраница 2
Таблицы термодинамических функций АЮ и А1Н, приведенные в первом и настоящем изданиях Справочника, идентичны. [16]
Таблицы термодинамических функций воздуха для температур от 200 до 6000 К и давлений от 0 00001 до 100 атм являются частью работ, посвященных исследованию свойств газов при высоких температурах, которые проводятся под общим руководством члена-корреспондента АН СССР профессора А. С. Предводителева в Лаборатории физики горения Энергетического института АН СССР и на кафедре молекулярной физики физического факультета Московского государственного университета. [17]
Таблицы термодинамических функций LiOH, приведенные в первом и настоящем изданиях Справочника, идентичны. [18]
Таблицы термодинамических функций LiF, приведенные в первом и настоящем изданиях Справочника, идентичны. [19]
Таблицы термодинамических функций воздуха для температур от 6000 до 12 000 К и давлений от 0 001 до 1000 атм являются частью работ, посвященных исследованию свойств газов при высоких температурах и проводимых под общим руководством члена-корреспондента АН СССР профессора А. С. Предводителева в лаборатории физики горения Энергетического института АН СССР и на кафедре молекулярной физики физического факультета Московского государственного университета. К настоящему времени коллективом лаборатории и кафедры составлены таблицы термодинамических функций воздуха для температур от 1000 до 20000 К, а также таблицы газодинамических и термодинамических величин потока воздуха за прямым [ скачком уплотнения и у поверхности конуса для скоростей набегающего потока до 15 500 м / сек. Таблицы термодинамических функций воздуха для температур от 6000 до 12 000 К являются первым томом из перечисленной выше серии таблиц. [20]
Таблицы термодинамических функций воздуха составлены для значений температур от 6000 до 12 000 К и значений давлений от 0 001 до 1000 атм. [21]
Таблицы термодинамических функций воздуха ( для температур от 6000 до 12 000 К и давлений от 0 001 до 1000 атм) / Предводителев А. [22]
Таблицы термодинамических функций двуокиси азота до 2000 К, приведенные в справочниках Келли [2363], Рибо [3426] и Цейзе [4380], основаны на расчете Джиока и Кемпа [1716], использовавших устаревшие в настоящее время значения основных частот NOa ( vi 1373, V2 641 HVa 1615 см 1) и произведения моментов инерции ( 14 4 - 10 - 117 г3 - смв), и поэтому сравнивать результаты, приведенные в табл. 98 ( II), с данными, имеющимися в указанных справочниках, нецелесообразно. Расчеты Морозова [303] ( Г1000 К) и Альтшуллера [530] ( 7X 1500 К) выполнены в приближении модели жесткий ротатор - гармонический осциллятор практически по тем же значениям основных частот, которые приняты в настоящем Справочнике. Расхождения между значениями, приведенными в табл. 98 ( II), и данными Альтшуллера, достигающие 0 4 кал / моль-град в значении 5150 возникают главным образом из-за учета ангармоничности колебаний и центробежного растяжения NO2 в настоящем Справочнике. [23]
Таблицы термодинамических функций двуокиси кремния, приведенные в первом и настоящем изданиях Справочника, идентичны. [24]
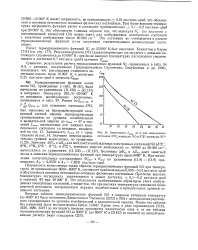 |
Зависимость Утах от v для электронного состояния Х2ПГ молекулы NO и Х1 1 молекулы N0. [25] |
Впервые таблица термодинамических функций NO в широком интервале температур ( до 5000 К) была составлена Джонстоном и Чапманом [2272] в 1933 г. методом непосредственного суммирования по уровням колебательной и вращательной энергии. Кроме того, в ряде справочников [ 2142, 3426, 3680, 3507 ] до последнего времени приводится практически одна и та же таблица термодинамических функций NO до 5000 К ( до 6000 К в [2142]) со ссылкой на неопубликованные расчеты Бюро стандартов США. [26]
По таблицам термодинамических функций гармонического осциллятора для данного значения 6 / Т находим Фг. [27]
Поэтому вычисление таблиц термодинамических функций веществ в твердом и жидком состояниях в настоящее время может быть проведено только на основании результатов экспериментальных измерений теплоемкости и теплот фазовых переходов с использованием соотношений, основанных на третьем законе термодинамики. [28]
Другие расчеты таблиц термодинамических функций двуокиси циркония в литературе неизвестны. [29]
Пояснительная записка к таблицам термодинамических функций АЬОз, С, F, N, NF, АЮ, Be, Н и LiH, Отч. [30]
Страницы: 1 2 3 4