Таблица - термодинамическая функция
Cтраница 3
Пояснительная записка к таблицам термодинамических функций CN, АЮ и LiH, Отч. [31]
Для расчетов воспользуемся таблицами термодинамических функций, концентраций компонент и ударных адиабат воздуха, в которых термодинамические функции и ударные адиабаты воздуха вычислены по формулам статистической теории газов и газодинамической теории ударных волн. [32]
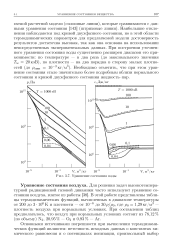 |
Уравнение состояния воды. [33] |
В этой работе представлены таблицы термодинамических функций, вычисленных в диапазоне температуры от 200 до 3 106 К и плотности - от 10 - 6 до ЗОр / ро, где р 1 29кг / м3 - плотность воздуха при нормальных условиях. [34]
 |
Значения постоянных для расчета термодинамических функций NH, NS и NF. [35] |
Приведенная в настоящем Справочнике таблица термодинамических функций NH идентична с приведенной в первом издании Справочника. [36]
 |
Значения постоянных для расчета термодинамических функций NH, NS и NF. [37] |
Приведенная в настоящем Справочнике таблица термодинамических функций NS полностью совпадает с таблицей, приведенной в первом издании. Другие расчеты термодинамических функций NS в литературе не известны. [38]
Предводите лев А. С. И др. Таблицы термодинамических функций воздуха для температур от 200 до 6000 К и давлений от 0 00001 до 100 атмосфер. [39]
Отдельно изложена мгтодика расчета таблиц термодинамических функций газов в настоящем Справочнике и приведены соотношения, позволяющие оценивать точность этих расчетов, а также методы аппроксимации табулированных значений термодинамических свойств полиномами. [40]
В литературе отсутствуют расчеты таблиц термодинамических функций полуокиси алюминия для широкого интервала температур. [41]
Эти составляющие находятся по таблицам термодинамических функций гармонического осциллятора ( см. стр. [42]
В последующие годы были изданы таблицы термодинамических функций и констант равновесия образования простых веществ 92 элементов ( от Н до U), вычисленные Сталлом и Зинке [3894] на основании исходных данных, опубликованных до 1956 г. Эти таблицы были вычислены как для элементов в кристаллическом и жидком состояниях ( 298 15 - точка кипения), так и для одноатомных и многоатомных газов в интервале 298 15 - 3000 К. [43]
В литературе по термодинамике приводятся таблицы термодинамических функций ( параметров) для стандартного состояния вещества. [44]
В 1961 г. была опубликована таблица термодинамических функций SOa, вычисленная Гордоном [ 1817а ] для Т - 298 15; 300 ( 100) 6000 К. Вычисления выполнены по методу Пеннингтона и Коба ( см. стр. До 1000 К соответствующие значения термодинамических функций SO2, приведенныев работе [ 1817а ] и в табл. 80 ( II), совпадают полностью. При более высоких температурах имеются систематические расхождения, связанные с использованием различных методов расчета ( различия в значениях Ф 000 и S6000 составляют 0 096 и 0 322 кал / мо. [45]
Страницы: 1 2 3 4