Тайрон
Cтраница 2
Тем же автором применен тайрон для хроматографического отделения железа, алюминия, титана от кальция, магния, марганца и меди. Метод основан на образовании комплексов Fe3, Al3 Ti4 с динатриевой солью пирокатехина 3 - 5-дисульфокис-лоты. [16]
Добавляют около 130 мг сухого тайрона в каждый стакан. [17]
Пирокатехиновый фиолетовый, как и тайрон, связывает металлы посредством двух фенолят-ионов, а в PAN этой цели служат пиридиновый азот, атомы азота азо-группы и ионизированная окси-группа. [18]
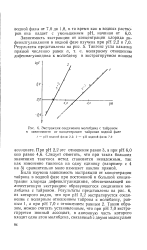 |
Экстракция соединения молибдена с тайроном в зависимости от концентрации тайронав водной фазе. [19] |
Была изучена зависимость экстракции от концентрации тайрона в водной фазе при постоянной и большой концентрации хлорида дифенилгуанидиния, обеспечивающей количественную экстракцию образующегося соединения молибдена с тайроном. [20]
Были изучены зависимости скорости реакции окисления тайрона перекисью водорода от рН среды и концентраций реагирующих веществ. [21]
Было установлено [19], что реакция окисления тайрона ( Н2Т) перекисью водорода протекает в две стадии. Для идентификации продуктов окисления тайрона были применены спектрофотометрический метод и метод тонкослойной хроматографии. На основании литературных данных [20, 21] и экспериментальных результатов можно предположить, что на первой стадии каталитического окисления тайрона образуется хинон ( тах 435 нм), на второй стадии имеет место димеризация и полимеризация хинона. Никель оказывает каталитическое действие на обе стадии реакции. [22]
Комплексные соединения молибдена с некоторыми мер-каптокислотами и тайроном экстрагируются в виде ионных ассоциатов с катионами дифенилгуанидиния или бензил-тиурония. [23]
Полагают, что в случае фенольных реагентов типа тайрона, применяемого для определения Fe3, Cu2 и V4 r так же как и в случае тиоуксусной и сульфосалициловой кислот, используемых для определения Fe3, характерные спектры их комплексов с металлами обусловлены переносом заряда с перемещением электрона от лиганда к иону металла. Приблизительно верно и то, что в комплексах различных металлов с данным лигандом полосы переноса заряда по мере усиления окислительной способности ионов металлов смещаются в область более длинных волн. Увеличение устойчивости высших степеней окисления при переходе сверху вниз; в каждой группе периодической системы элементов ( например Fe - - Ru - - Os) приводит по тем же причинам к увеличивающемуся сдвигу соответствующих полос в область более коротких длин волн. Это, видимо, справедливо и для окрашенных комплексов, образуемых алкилами бериллия и его галогенидными соединениями с а, а - дипиридилом, комплексов алкилов Zn, Cd, A1 и Ga с а, а - дипиридилом и для аналогичных комплексов, образуемых алкилами Be, Zn, CdT А1 и Ga с ароматическими аминами. [24]
К таким реагентам относятся дибензоилметан, хромо-троповая кислота, тайрон, салициловая кислота, сульфосалицило-вая кислота, ализариновый красный S, торон, морин и крезотино-вая кислота. В отсутствие хрома ( VI) ( если он присутствует, то его необходимо восстановить) и галогенидов, приводящих к экстракции других ионов, реакцию с дибензоилметаном можно сделать специфичной для урана, проводя предварительную его экстракцию. [25]
Никель может быть определен по каталитической реакции: дифенил-карбазон - тайрон - перекись водорода. Определение никеля в присутствии кобальта рекомендуется проводить с предварительной экстракцией хлороформом комплексного соединения никеля с диметилглиоксимом. [26]
 |
Термодинамические характеристики активированного состояния. [27] |
Из полученных данных видно, что при введении в систему тайрон - Н202 катализатора Ni2 происходит резкое уменьшение свободной энергии активации AG, что облегчает протекание окислительно-восстановительной реакции. АН) - энтальпия - практически не изменяется, что свидетельствует в пользу внутрикомплексного механизма при промежуточном комплексообразовании. [28]
При прибавлении к растворам солей уранила пирокатехина, пирогаллола, тайрона ( пиро-катехиндисульфокислоты), хромотроповой кислоты ( 1 8-диоксинафта-лин - 3 6-дисульфокислоты) и других соединений этого типа растворы приобретают красно-оранжевую, красно-коричневую или коричневую окраску. При этом чаще всего образуются одноядерные хелаты. Исследование системы UO1 - пирокатехин фотометрическим методом показало, что в этой системе образуется ряд одноядерных комплексов с отношением компонентов UO2: R. Для фотометрического определения урана эти комплексообразующие реагенты малоудобны. [29]
Наибольшее применение получили реакции окисления пероксидом водорода ализарина С, тайрона и пирокатехина. [30]
Страницы: 1 2 3 4