Сильное изменение - концентрация
Cтраница 1
Сильное изменение концентрации N0 атомов примеси в зоне разряда может привести к переходу от одной части кривой роста к другой; это вызовет изменение наклона кривой. [2]
В связи с сильным изменением концентрации аниона реагента при повышении кислотности на кривых экстракции могут появляться минимумы. Появление минимумов на кривых экстракции пиразолиндитиокарбаминатов металлов, имеющих несколько валентных состояний, связано в ряде случаев с изменением окислительно-восстановительных потенциалов. Минимумы на кривых экстракции могут иметь место также при изменении ионного состояния элементов в растворах. [3]
В полидисперсных системах при седиментационном равновесии у крупных частиц наблюдается более сильное изменение концентрации с высотой, чем у мелких. [4]
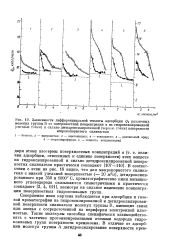 |
Зависимости дифференциальной теплоты адсорбции Qa различных. [5] |
С, хроматографические пики насыщенного углеводорода оказываются симметричными и практически совпадают [3, 4, 111], несмотря на сильное изменение концентрации поверхностных гидроксильных групп. [6]
 |
Триггериый режим в модели гликолиза. [7] |
Дынник, Сельков и Семашко ( 1972) исследовали модель, учитывающую, в отличие от (5.12), возможность сильных изменений концентрации АТФ. [8]
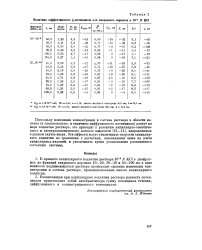 |
Величина эффективного g - потенциала для кварцевого ворошка в 10 - 3 У КС1. [9] |
В процессе капиллярного поднятия раствора 10 - 3 N КС1 в диафрагмах из фракций кварцевого порошка 10 - 20, 20 - 50 и 50 - 100 мк в зоне менисков поднимающегося раствора происходят сильные изменения концентрации и состава раствора, пропорциональные высоте капиллярного поднятия. [10]
В случае кислой реакции к жидкости прибавляют допо. Чтобы избежать сильного изменения концентрации бордосской жидкости против заданной, для усреднения следует брать концентрированное известковое молоко, например 10 - In о-мое. [11]
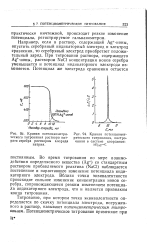 |
Кривая потенциометри-ческого титрования раствора нитрата серебра раствором хлорида натрия.| Кривая потенциомет-рического титрования, построенная в системе координат. [12] |
Во время титрования по мере взаимодействия определяемого вещества ( Ag) со стандартным раствором прибавляемого реактива ( NaCl) наблюдается постепенное и нарастающее изменение потенциала индикаторного электрода. Вблизи точки эквивалентности происходит сильное изменение концентрации ионов серебра, сопровождающееся резким изменением потенциала индикаторного электрода, что и является признаком конца титрования. [13]
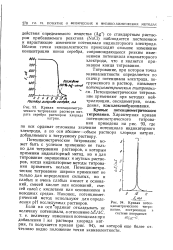 |
Кривая потен. [14] |
NaCl) наблюдается постепенное и нарастающее изменение потенциала индикаторного электрода. Вблизи точки эквивалентности происходит сильное изменение концентрации ионов серебра, сопровождающееся резким изменением потенциала индикаторного электрода, что и является признаком конца титрования. [15]
Страницы: 1 2 3
