Сильное изменение - концентрация
Cтраница 3
Изменение концентрации спирта в конденсате также требует корректировки режима ректификации - как в отборе дистиллята, так и в подаче флегмы и пара в кипятильники. Температура куба и верха колонны при этом не меняется. При нормальном режиме гидратации сильных изменений концентрации спирта в конденсате обычно не бывает. [31]
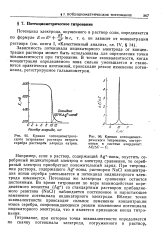 |
Кривая потенциометриче-ского титрования раствора нитрата серебра растворам хлорида натрия.| Кривая потенциомет-рического титрования, построенная в системе координат. Л. / ДС - С. [32] |
Например, если в раствор, содержащий А § - ионы, опустить серебряный индикаторный электрод и электрод сравнения, то серебряный электрод приобретает положительный заряд. При титровании раствора, содержащего Ag - HOHbi, раствором NaCl концентрация ионов серебра уменьшается и потенциал индикаторного электрода изменяется. Потенциал же электрода сравнения остается постоянным. Во время титрования по мере взаимодействия определяемого вещества ( Ag) со стандартным раствором прибавляемого реактива ( NaCl) наблюдается постепенное и нарастающее изменение потенциала индикаторного электрода. Вблизи точки эквивалентности происходит сильное изменение концентрации ионов серебра, сопровождающееся резким изменением потенциала индикаторного электрода, что и является признаком конца титрования. [33]
Например, если в раствор, содержащий Ag, опустить серебряный индикаторный электрод и электрод сравнения, то серебряный электрод приобретает положительный заряд. При титровании раствора, содержащего Ag, раствором NaCl концентрация ионов серебра уменьшается и потенциал индикаторного электрода изменяется. Потенциал же электрода сравнения является постоянным. Поэтому во время титрования по мере взаимодействия определяемого вещества ( Ag) со стандартным раствором прибавляемого реактива ( NaCl) наблюдается постепенное и нарастающее изменение потенциала индикаторного электрода. Вблизи точки эквивалентности происходит сильное изменение концентрации ионов серебра, сопровождающееся резким изменением потенциала индикаторного электрода, что и является признаком конца титрования. [34]
 |
Потенциал каломельного электрода. [35] |
Например, если в раствор, содержащий Ag - HOHbi, опустить серебряный индикаторный электрод и электрод сравнения, то серебряный электрод приобретает положительный заряд. При титровании раствора, содержащего Ag - HOHbi, раствором Nad концентрация ионов серебра уменьшается и потенциал индикаторного электрода изменяется. Потенциал же электрода сравнения является постоянным. Поэтому во время титрования по мере взаимодействия определяемого вещества ( Ag) со стандартным раствором прибавляемого реактива ( NaCl) наблюдается постепенное и нарастающее изменение потенциала индикаторного электрода. Вблизи точки эквивалентности происходит сильное изменение концентрации ионов серебра, сопровождающееся резким изменением потенциала индикаторного электрода, что и является признаком конца титрования. [36]
 |
Потенциал каломельного электрода. [37] |
Например, если в раствор, содержащий Ag - noHbi, опустить серебряный индикаторный электрод и электрод сравнения, то серебряный электрод приобретает положительный заряд. При титровании раствора, содержащего Ag - HOHbi, раствором NaCI концентрация ионов серебра уменьшается и потенциал индикаторного электрода изменяется. Потенциал же электрода сравнения является постоянным. Поэтому во время титрования по мере взаимодействия определяемого вещества ( Ag) со стандартным раствором прибавляемого реактива ( NaCI) наблюдается постепенное и нарастающее изменение потенциала индикаторного электрода. Вблизи точки эквивалентности происходит сильное изменение концентрации ионов серебра, сопровождающееся резким изменением потенциала индикаторного электрода, что и является признаком конца титрования. [38]
Страницы: 1 2 3