Температура - диссоциация - карбонат
Cтраница 1
Температуры диссоциации карбонатов таковы: кальцит - 920 - 940 С, доломит - 750 - 760 С и 930 - 940 С. [1]
Температура диссоциации карбоната кальция лежит в пределах 850 - 920, ввиду этого механическая прочность гранул при температурах 400 - 600 сохраняется. [2]
 |
Термограмма карбоната кальция в смеси с Са ( ОН а при различных величинах навесок СаС03 ( пунктир. [3] |
Еще более противоречивы литературные данные о температуре диссоциации карбоната магния. [4]
 |
Определение температуры плавления по кривой нагревания.| Определение температуры плавления по кривой охлаждения. [5] |
Неоценимые услуги кривые нагревания оказывают при определении температур диссоциации карбонатов и обезвоживания гидратов. Однако и в этих случаях приходится считаться с тем, что на получаемые температурные значения изучаемых эффектов влияют скорость нагревания, величина навески, теплопроводность, теплоемкость испытуемого вещества и тому подобные факторы. [6]
 |
Определение температуры плавления по кривой нагревания. [7] |
Неоценимые услуги кривые нагревания оказывают при определении температур диссоциации карбонатов и обезвоживании гидратов. [8]
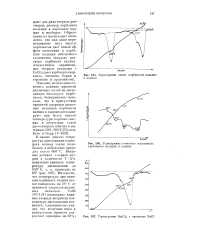 |
Термограмма смеси карбонатов кальция и кадмия.| Термограмма совместно осажденных карбонатов кальция и кадмия.| Термограмма MgC03 с примесью NaCl. [9] |
Интересно, что температура диссоциации карбоната кадмия также снижалась на 60 С от примесей хлоридов щелочных металлов. [10]
Реакция между свободной кремнекислотой и карбонатом кальция впервые была тщательно изучена Коб - бом27, особенно в случае взаимодействия при нагревании осажденного карбоната кальция с кварцем при атмосферном давлении. Взаимодействие начинается в твердой фазе при температуре около 800 С, которая немного ниже температуры диссоциации карбоната, независимо от количественных соотношений компонентов. После нагревания в течение нескольких часов карбонат уже не обнаруживается. Если в смеси имеется избыток извести, то, согласно Коббу, в результате образуется двукальциевый силикат; но если имеется избыток кремнезема, то возникает метасиликат кальция. [11]
Различие в поляризации связей Me-О и О-С с температурой уменьшается, что и приводит в конце концов к диссоциации. Эта контрполяризация в ряду однотипных ионов ( например, Са2 - Sr2 - Ва2) ослабевает, что и объясняет повышение температуры диссоциации соответствующих карбонатов. Контрполяризация может стать столь значительной, что соединение может оказаться устойчивым только при очень низких температурах. [12]
Различие в поляризации связей Me-О и О-Gc температурой уменьшается, что и приводит в конце концов к диссоциации. Эта контрполяризация в ряду однотипных ионов ( например, Са2 - St2 - Ваг) ослабевает, что и объясняет повышение температуры диссоциации соответствующих карбонатов. Контрполяризация может стать столь значительной, что соединение окажется устойчивым только при очень низких температурах. [13]
Это свидетельствует о том, что присутствующая в газе двуокись углерода не оказывает влияния на скорость этой реакции. Кроме того, при 1000 С и наличии в газе двуокиси углерода не наблюдается сколько-нибудь заметного взаимодействия последней с окисью кальция, так как указанная температура выше температуры диссоциации карбоната кальция. Изменения скорости прямого взаимодействия сероводорода с окисью кальция в присутствии двуокиси углерода не происходит. [14]
Тамман и Пейп u объяснили это увеличение стойкости глинозема в продуктах разложения каолина при более высоких температурах начинающейся рекристаллизацией окиси. Они обнаружили, в соответствии с этим предположением, что как чистый глинозем, так и глинозем, который присутствует в разложившемся каолине при температуре выше 550 С, понижают температуру диссоциации карбонатов щелочноземельных металлов ( при давлении в il атм) приблизительно на 220 С. Если нагревать тонкую механическую смесь кремнезема и глинозема, то при температуре 940 С наблюдается положительный тепловой эффект, который, очевидно, имеет тот же характер, что и соответствующий экзотермический эффект в каолине. В обоих Случаях растворимость глинозема в кислотах сильно уменьшается. [15]
Страницы: 1 2